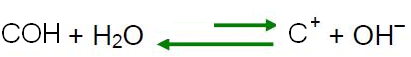
媒体が同じ濃度(mol / L)のヒドロニウムイオン(H3O+)および水酸化物(OH-).
他の溶液の標準としても機能する中性媒体の例は、25ºCの温度の純粋な蒸留水です。 この温度では、正確に1になります。 10-7 両方のイオンのmol / L。 したがって、あなたのイオン生成物(Kw)は10に等しい-14 (mol / L)2:
Kw = [H3O+]. [おお-]
Kw = (1. 10-7 mol / L)。 (1. 10-7 mol / L)= 10-14 (mol / L)2
pHとpOHを以下に示します。
pH = --log [H3O+] pOH = -log [OH-]
pH = --log1。 10-7 pOH = --log1。 10-7
pH = 7pOH = 7
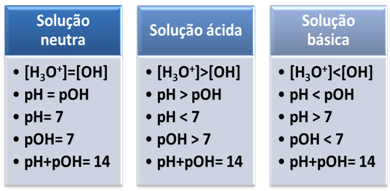
これは、中立的なソリューションでは、 pHはpOHに等しい.
- 酸性培地:
酸性媒体では、Hイオンの濃度3O+ OHイオンよりも大きい-.
このような解決策は、Hイオンのごく一部を追加することで実現できます。3O+、例えば、酸による。
ルシャトリエの原理によれば、平衡状態にあるシステムに外乱が発生すると、この力の影響を減らすためにシステムが再調整される傾向があります。 これは、酸が水に加えられると、Hイオンが3O+ それらは過剰になり、バランスは逆反応方向に左にシフトします。 したがって、これらの過剰なイオンはOHイオンと反応します-. したがって、OHイオンの濃度- 減少し、溶液は酸性になります。

イオン生成物(Kw)は常に10に等しい-14、しかしHイオンの濃度3O+ OHイオンの濃度よりも大きい-1. したがって、pHは酸性媒体のpOHよりも高くなりますが、その合計は常に14に等しくなります。
また、Hイオンの濃度が高いほど3O+、pH値が大きいほど。 室温(25°C)、pH <7およびpOH> 7。

- 基本的な意味:
塩基性培地では、OHイオンの濃度- Hイオンよりも大きい3O+.
水に塩基を加えると、OHイオンを加えることになります。- そして、前の項目で説明したように、ルシャトリエの原理により、 水の自己イオン化は反対方向に移動し、過剰なイオンが Hイオン3O+、あなたの集中力を減らし、解決策を基本的にします。
その場合、pOHはpHよりも大きくなります。 室温(25°C)、pH> 7およびpOH <7。

簡単に:
ジェニファー・フォガサ
化学を卒業

