構造式は、構造、つまり、化学元素を構成する原子の配置、およびそれらの間の接続を示すスキームです。 フラット、コンデンス、エレクトロニックなど、さまざまな方法で表現できます。
使用される構造を条件付ける要因の中で、価電子シェル内の電子の数はそれらの1つです。
フラット式
フラット式では、ダッシュを使用して共有結合を表します。共有結合は、単一、二重、または三重であり、次のように表されます。
–簡単な接続 (2つの電子が共有されている場合)
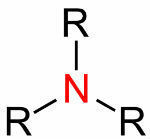
=二重結合 (4つの電子が共有されている場合)
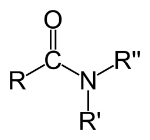
≡トリプルリンク (6つの電子が共有されている場合)
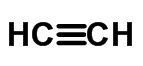
凝縮または簡略化された式
凝縮された構造式では、結合は示されていません。
その表現では、各元素の原子数は凝縮された方法で示されます。つまり、簡略化されています。
H3C CH2 CH2 CH3
線形凝縮式
線形凝縮式はジグザグ線を使用し、その頂点で炭素が表されます。
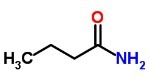
電子式またはルイス式
ルイス式とも呼ばれる電子式は、ドットで表されます。
これらの点を通して、原子価層に存在する電子の量が示されます。
H:H
そして分子式?
THE 分子式は、その構造を参照せずに、を構成する要素の数を示します 分子. 各元素に存在する原子の数とそれらの比率を示すことに加えて。
これは、最小または実験式とパーセンテージまたは百分率の式から取得できます。
あまりにも読む 異性 そして バレンシア層.
解決された演習
1. (Vunesp-2000)構造式を書き、正式な名前を付けます。
a)合計7個の炭素原子を有する飽和分岐炭素鎖ケトン。
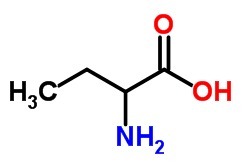
b)4つの炭素原子を持つアミノ酸。
)

B)
2. (FGV-2005)アスパルテームは、1965年に不注意な化学者が汚れた指をなめ、甘いと感じて偶然発見した人工甘味料です。
微量の多くの物質は非常に有毒であるため、これらの非衛生的な習慣は推奨されません。
アスパルテームの構造式を以下に示します。

アスパルテームの構造式から、
a)分子あたり13個の炭素原子。
b)1つのエーテル官能基。
c)1つのジペプチド
d)2つの三級炭素原子
e)1つの不斉炭素原子のみ。
代替c:1ジペプチド
知識のテストを続けるには、次の演習リストも参照してください。
- 炭化水素に関する演習
- 有機化学の演習
- フラット異性に関する演習



