顕熱または敏感な比熱は、体温の変化に関連する物理量です。
例:金属棒の加熱
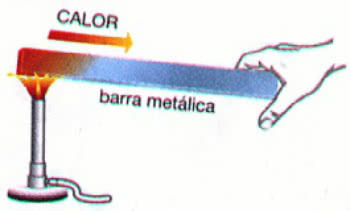
上記の例では、熱は 熱伝導. このプロセスにより、材料の温度が上昇しますが、その物理的状態は同じ(固体)のままです。
式
顕熱を計算するには、次の式を使用します。
Q = m。 ç。 Δθ
Q:顕熱量(ライムまたはJ)
m:体重(gまたはkg)
ç:物質の比熱(cal / g°CまたはJ / Kg°C)
Δθ:温度変化(°CまたはK)
注意:顕熱を計算するには、各物質で変化する比熱を知る必要があります。
続きを読む: 比熱.
顕熱と潜熱
で 潜熱 (L)、物質の物理的状態は変化しますが、顕熱では同じままです。
2つの違いのもう1つは、温度に関するものです。 つまり、潜熱は体温に依存しませんが、顕熱はそれを考慮します。
潜熱の例は、角氷の融解または水の蒸発です。 どちらの場合も、2つの物理状態の温度は同じままです。
潜熱を計算するには、次の式を使用します。
Q = m。 L
どこ、
Q:熱量(ライムまたはJ)
m:質量(gまたはkg)
L:潜熱(cal / gまたはJ / Kg)
あまりにも読んでください:
- 熱と温度
- 熱量測定
- 熱バランス
- 熱容量
- 物理式
フィードバック付き入試演習
1. (マッケンジー)熱源は、与えられた質量の水に150 cal / sの速度で継続的に熱を供給します。 水温が4分で20°Cから60°Cに上昇し、水の比熱感受性が1.0 cal / g°Cである場合、加熱された水の質量(グラム)は次のように結論付けることができます。
a)500
b)600
c)700
d)800
e)900
代替および
2. (UFSM-RS)400 gの本体と、10°Cの温度で0.20 cal / g°Cの敏感な比熱が配置されます 別の200gの物体と熱接触し、0.10 cal / g°Cの敏感な比熱で、 60°C。 2つの物体間の熱バランスが確立されると、最終的な温度は次のようになります。
a)14°C
b)15°C
c)20°C
d)30°C
e)40°C
代替案c
3. (UFPR)日食の間、全体ゾーンの都市の1つであるクリシウマ-SCで、8.0°Cの温度低下がありました。 (ゼロアワー– 1994年11月4日)
水の敏感な比熱が1.0cal / g°Cであることを知っていると、石灰で温度を8.0°Cから下げたときに1000gの水から放出される熱量は次のとおりです。
a)8.0
b)125
c)4000
d)8000
e)64000
代替案