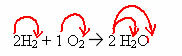pHは水素イオンポテンシャルを表し、pOHは溶液のヒドロキシイオンポテンシャルを表します。
これらは、サンプルの酸性および塩基性の特性を測定するために使用される対数目盛です。
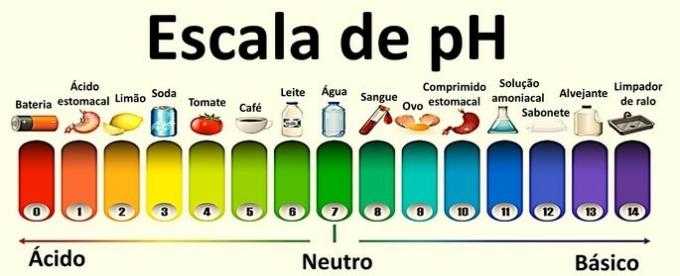
それらを構成する値は0から14の範囲であり、水のイオンバランスから得られました。
中性溶液のpHは7です。 7未満の値は溶液を酸性として分類し、7を超えると溶液は塩基性に分類されます。
pH値を使用すると、減算するだけで、pOHスケールで対応する値を見つけることができます。
イオン水収支
水分子には、次の式に従ってイオン化する能力があります。
ここでは、イオンのバランスが取れています。これは、プロセスが可逆的であり、イオンが集まって水分子を再び形成する可能性があるためです。
発生するバランスを示す別の方法は、 自動イオン化.
水分子はヒドロニウムイオン(H3O+)およびヒドロキシル(OH-)2番目の分子の破壊を介して。
水のイオン積(Kw)
水のイオンバランスの定数は次のとおりです。
水は純粋な液体であるため、その濃度は1と見なされ、定数値に干渉しません。 したがって、式は次のようになります。
O のイオン生成物 水 é .
この式は記号Kを受け取りますw (Wは英語の単語waterから来ています- 水)そして平衡定数のように、それは温度によって変化します。

pHとpOHの決定
25°Cの温度では、水のイオン積は次のとおりです。
純水のイオン化では、1molのH3O+ 1molのOHで形成されます- .
すぐに、
これらの値は非常に低いため、符号が入れ替わった対数に対応する対数の値を使用することにしました。
水のイオン積にコロガリズムを適用するには、次のことを行う必要があります。
溶液のpHがわかっている場合、14から最初の値を引くことでpOH値を見つけることができます。
溶液の酸性度と塩基性度
ニュートラルソリューション:ヒドロニウムイオンの濃度は、ヒドロキシルの濃度と同じです。
| [H3O+] = 1,0. 10-7 mol / L | pH = 7 |
| [ああ-] = 1,0. 10-7 mol / L | pOH = 7 |
例:純水。
酸性溶液:ヒドロニウムイオンの濃度がヒドロキシルの濃度よりも高い。
| [H3O+] |
pH |
| [ああ-] |
pOH |
例:ソーダ、レモン、トマト。
基本的な解決策:ヒドロキシルの濃度がヒドロニウムイオンの濃度よりも高い。
| [H3O+] |
pH |
| [ああ-] |
pOH |
例:卵、石鹸、漂白剤。
pH計算
水素ポテンシャルの概念は、デンマークの化学者Peter Lauritz Sorensen(1868-1939)によって作成され、Hの濃度によって溶液の酸性度を表現しました。+.
のイオン化を示す以下の表を参照してください。 酸:
| 初期モル濃度 | 0,020 | 0 | 0 |
| イオン化 | 0,001 | 0,001 | 0,001 |
| バランスのとれたモル濃度 | 0,019 | 0,001 | 0,001 |
この例では、Hイオンの濃度が+ é 0,001. したがって、溶液のpHは次のとおりです。
[H+] = 0,001 = 10-3
pH = --log 10-3 = 3
溶液のpHが7未満であるため、この溶液は酸性です。
pHとpOHのまとめ
| 定義 | pH:溶液の水素イオンポテンシャル。 | |
|---|---|---|
| pOH:溶液のヒドロキシルイオンポテンシャル。 | ||
| 一般式 | pH + pOH = 14 | |
| ソリューション | 中性 | pH = pOH = 7 |
| 酸性 |
pH pOH> 7 |
|
| 基本 |
pOH pH> 7 |
|
| pH計算 | pH = --log [H+] | |
| pOHの計算 | pOH = -log [OH-] |
pHとpOHに関する演習
1. (FMTM)塩酸(HCℓ)の水溶液である胃液のpHは約2です。 したがって、胃液1リットルあたりに存在するHCℓの質量(グラム単位)は次のようになります。
データ:モル質量(g / mol)H = 1、Cℓ= 35.5
a)7.3・10-2
b)3.65・10-1
c)10-2
d)2
e)10
正しい代替案:b)3.65・10-1.
最初のステップ:Hイオンの濃度を計算します+.
2番目のステップ:HClのモル質量を計算します。
3番目のステップ:胃液1リットルあたりの塩酸の質量を計算します。
2. (UEMG)いくつかの洗浄剤は、その構成にアンモニアが含まれています。 これらの製品の1つのラベルは、pH = 11を示しています。 これは、この製品のヒドロキソニウムカチオンとヒドロキシルアニオンの濃度がそれぞれ次のとおりであることを意味します。
1に。 10-3 および1。 10-11
b)1。 10-11 および1。 10-7
c)1。 10-11 および1。 10-3
d)1。 10-11 および1。 10-11
正しい代替案:c)1。 10-11 および1。 10-3.
a)間違っています。 これらの濃度は、pH = 3の溶液に対応します。
b)間違っています。 Hの濃度が+ 溶液のpHが11、OHイオンの濃度であることを示します- pOH = 14-pHであるため、3である必要があるため、間違っています。
c)正しい。 pH + pOH = 14であるため、pH = 11およびpOH = 3。
d)間違っています。 Hの濃度が+ 溶液のpHが11、OHイオンの濃度であることを示します- pOH = 14-pHであるため、3である必要があるため、間違っています。
a)0.1 mol / L NaOH
b)NaCl 0.5 mol / L
c)H2のみ4 1.0 mol / L
d)1.0 mol / L HCl
e)0.2 mol / L KOH
正しい代替案:e)KOH 0.2 mol / L。
a)間違っています。 この溶液は、pHが7より大きいため塩基性ですが、代替品のpHが高くなることはありません。
b)間違っています。 NaClは強酸塩基反応の生成物であるため塩です。 したがって、そのpHは中性です。
c)間違っています。 硫酸は強酸であるため、pHが低くなります。
d)間違っています。 塩酸は強酸であるため、pHが低くなります。
e)正しい。 pHが7より大きいため、溶液は塩基性です。