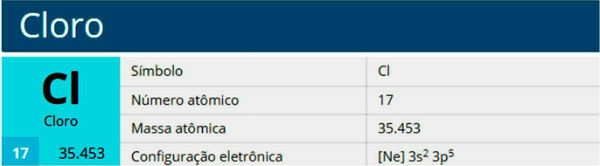
塩素は、記号Cl、原子番号17、原子量35.5の化学元素です。 ハロゲン族、グループ17または7A、および周期表の3番目の周期に属します。
その名前はギリシャ語に由来します khloros、これは緑がかったことを意味します。 これは、通常の温度と圧力の条件下では、塩素は強い臭いのある緑がかった黄色のガスとして特徴付けられるためです。
特徴
塩素は、1774年にスウェーデンの科学者カールヴィルヘルムシェール(1742-1786)によって発見されました。 しかし、当時は酸素との化合物だと思っていました。 1810年、ハンフリーデービー(1778-1829)は、それが新しい化学元素であることを示しました。
非常に反応性の高い元素であるため、火山の噴火時にHClの形で放出される少量を除いて、純粋な形で自然界に存在することはほとんどありません。
したがって、それは一般的に食卓塩としても知られている塩化ナトリウム(NaCl)の形で見られます。 鉱物では、カーナライトとシルバイトの形で発生します。
それはまたによって得ることができます 電解 水溶液中のNaClの。 塩素はまた、次のプロセスを通じて塩化物から多くの塩を生成します 酸化.
詳細については、以下もお読みください。
- 周期表
- 化学元素
- ハロゲン
アプリケーション
塩素ガス(Cl2)は有毒で刺激性があり、この状態により、第一次世界大戦中に化学兵器として使用されました。 このガスは、気道や皮膚の炎症、肺の水分貯留、裂傷を引き起こし、大量に吸入すると死に至る可能性があります。
塩素の他のいくつかの用途は次のとおりです。
- 二酸化塩素(ClO)を使用した紙や布地の漂白2).
- 水処理、塩素の添加は水を飲みやすくし、人間の消費に適したものにします。 このプロセスは塩素処理と呼ばれ、次亜塩素酸(HClO)を使用します。
- 塩素は微生物を殺すことができるので、プールの水と産業廃棄物の消毒。
- PVC(ポリ塩化ビニル)や合成ゴムなどのプラスチックコンパウンドの製造。
- いくつかの種類の有機および無機化合物の生産。

