原子体積は、原子が占める体積ではなく、 化学元素の特定の数の原子の固定量が占める体積。
本文中 化学元素、元素は、同じ原子番号、つまり原子核内の同じ量の陽子を持つ原子のセットに対応することが示されました。 原子体積を計算するために確立された量は、 アボガドロ定数、これは6.02に相当します。 1023 原子、これは元素の1モルに相当します。
だから私たちはそれを言うことができます 原子の体積は、1モルの原子(または6.02)の体積です。 1023 元素の原子)が占める。
この量は、固体元素の密度とその元素の1モルの原子の質量がわかっている場合に計算できます。 たとえば、ナトリウム(Na)の密度が0.97 g / cmに等しいとします。3 そしてその6.02。 1023 ナトリウム原子の質量は23.0gです。 次に、密度の式から、ナトリウムの原子体積に到達できます。 方法をご覧ください:
密度= パスタ
ボリューム
原子体積= 6.02の質量。 1023 元素原子
固体元素密度
ナトリウムの原子体積= 23.0 g
0.97 g / cm3
ナトリウムの原子体積= 23.71 cm3
原子の体積値には、原子のサイズだけでなく、原子間の距離も含まれます。 したがって、空きスペースも含まれるため、 できない 原子の体積値を取り、原子の数(6.02)で割ります。 1023)各原子が占める体積を見つける。
今やめないで... 広告の後にもっとあります;)
原子体積は周期的な性質であるため、元素の原子番号によって変化するため、原子体積を調べることが重要です。 下の画像を見てください。 元素の原子体積 上から下に成長しますつまり、周期表の同じファミリーに属する元素を分析すると、原子番号が大きくなると、原子体積も大きくなります。 これは、この意味で、周期が増加するためです。つまり、原子の電子層が増加し、その結果、原子が占める体積も増加します。 これはと同じ成長感です 原子線.
一方、水平方向では、原子体積が 中心から端に向かって増加します。 左から始めて、周期表の真ん中に右に行くと、周期が次のようになるため、原子体積が減少します。 同じ、つまり、同じ線の要素は同じ量の電子層を持っていますが、原子番号は 増加しています。 これは、電子の量がこの方向に増加することを意味し、その結果、 原子核への電子の引力により、原子半径が減少し、その結果、体積が減少します。 アトミック。 しかし、中央から右に向かって、これは継続しません。なぜなら、この領域にある要素の場合、 特に非金属の場合、それらの原子間の間隔は比較的大きく、原子の体積に影響を与えます。 それを増やす。
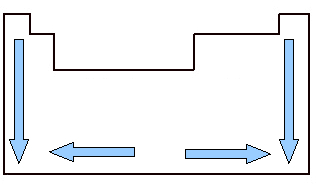
家族および期間にわたる周期表の原子体積変動
ジェニファー・フォガサ
化学を卒業