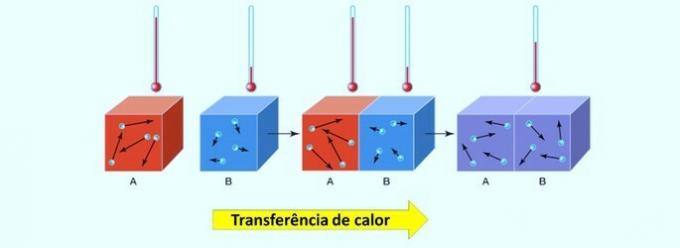
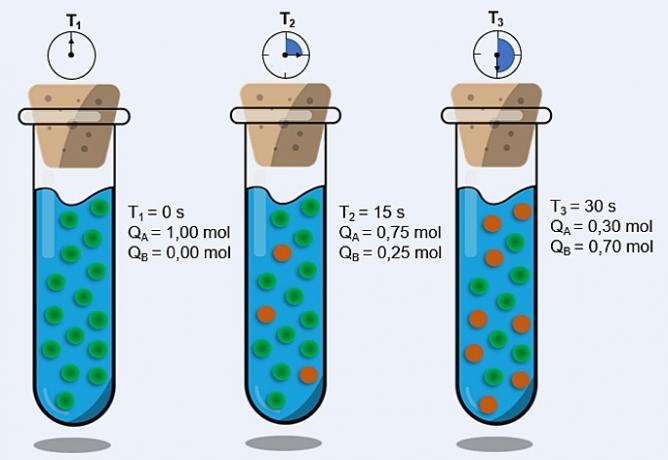
で 分子間力 それらは静電引力であり、その機能は分子(分子化合物)を結合し、それらを固体または液体状態に保つことです。 それらはすべての物理的特性を決定するため、非常に重要です(融点、沸点、密度および溶解度)物質の。
このテキストでは、 分子間力と物質の沸点との関係. 最初に、次の3つの重要なタイプの分子間力を思い出してみましょう。
♦ ダイポールダイポール:極性分子で発生する力です。 これらの分子には正と負の極があるため、双極子-双極子力は、ある分子の正の端と別の分子の負の端の間の引力に基づいています。 例:HCl、HBr、SO2 およびPH3
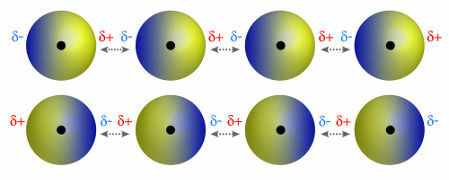
正極と負極が互いに引き合う分子
♦ 誘導双極子:は、非極性分子でのみ発生する分子間力です(極はありません)。 2つの無極性分子が近づくと、それらの雲の瞬間的な変形が発生します 電子は、分子の電子の不均衡を引き起こします。 彼女にとっては違う。 その瞬間、瞬間的な双極子が作成され、分子は瞬間的に正と負の極を持ち、それが引力を引き起こします。 例:CO2、CH4 およびBH3
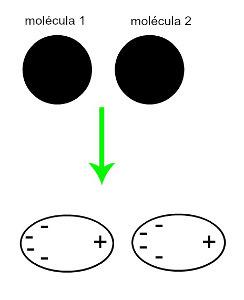
2つの非極性分子の近似により、変形が発生し、その結果、電子の再分布が発生し、瞬間的な双極子が形成されます。
♦ 水素結合:極性分子で発生するのは分子間力ですが、水素原子がフッ素、酸素、または窒素原子と直接結合している必要がある分子間力のみです。 これは双極子-双極子力と見なすことができますが、強度ははるかに大きくなります。 相互作用は常に、ある分子の水素と別の分子の異なる原子(F、O、N)の間で発生します。 例:H2O、NH3 およびHF
今やめないで... 広告の後にもっとあります;)
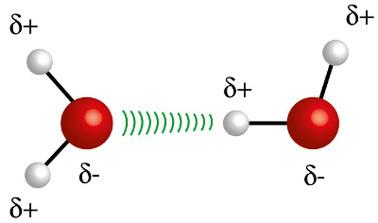
ある分子の水素原子(白い球)が別の水分子の酸素(赤い球)と相互作用します
3つの分子間力を思い出したので、これらを物質の沸点に関連付けることができます。 と呼ばれる 沸点 特定の物質の分子が液体状態でなくなり(分子間力が破壊され)、気体状態に切り替わる温度。 興味深い詳細は、 分子間力と沸点 分子間力が強いほど沸点が高くなるため、物質の割合は非常に強く直接的な関係にあります。 分子間力の強度の順序は次のとおりです。
誘導双極子
したがって、相互作用力として水素結合を持つ分子は、双極子-双極子などを持つ分子よりも沸点が高いと結論付けることができます。 以下の表は、3つの物質とそれらの沸点値を示しています。
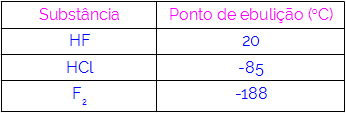
表では、HFの分子が水素結合によって結合されているため、HFの沸点が高いことがわかります。 物質F2 その分子は誘導された双極子に引き付けられるため、沸点が最も低くなります。
私によって。DiogoLopesDias
学校や学業でこのテキストを参照しますか? 見てください:
DAYS、ディオゴロペス。 "分子間力と物質の沸点"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/forcas-intermoleculares-ponto-ebulicao-das-substancias.htm. 2021年6月27日にアクセス。
化学
分子物質、沸騰温度、接触面、沸点、分子間引力、 化学結合、分子化合物、共有化学結合、イオン結合、金属結合、の物理的状態 悪い