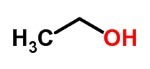
で 化学式 は、どの化学元素が物質の組成の一部であるかを示し、また関与する原子間の相互作用のタイプを表すために使用される表現です。
の分析を通じて 化学物質の式、 化学結合の性質を判断できます(イオン性, 共有結合 または金属)それを形成した、およびその物理化学的挙動。 物質の物理化学的挙動に関連するいくつかの特性は次のとおりです。
溶解性
融点
沸点
反応性
これで、化学物質を構成する化合物の種類と、それらを表す式がわかりました。
化合物の種類
) イオン性化合物
イオン性化合物はすべて、原子間のイオン結合によって形成される化学物質です。つまり、これらの化合物には、電子を失う原子と得る原子があります。 このタイプの化合物を形成する化学元素の組み合わせは、次のようになります。
金属 金属で
水素を含む金属
b)共有化合物
共有化合物はすべて、原子間の共有結合によって形成される化学物質です。つまり、これらの化合物には、互いに電子を共有する原子があります。 このタイプの化合物を形成する化学元素の組み合わせは、次のようになります。
ametalからametal
水素を含む非金属
水素と水素
c)金属化合物
金属化合物はすべて、単一の金属元素の原子によって形成される化学物質です。 これらの化合物では、原子は互いに電子を共有するだけです。
イオン性化合物の式
) イオン式
式イオンは、塩化物の場合のように、化合物のイオン単位を形成する原子の数を示します ナトリウムの式イオンはNaClです。 式では、ナトリウム原子と次の原子の存在を識別します。 塩素。
イオン式を作成するには、イオン性化合物を構成する各イオンの電荷を交差させるだけです。 アルカチオンの場合+3 と陰イオンO-2たとえば、電荷を交差させて信号を無視すると、次の式が得られます。
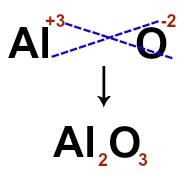
b)電子式
電子式は、化合物の形成に関与する原子の電子の損失と増加を表すために使用されます。 各元素の略語の周りに、私たちはの電子のそれぞれを持っています 原子価層.
塩化ナトリウム(NaCl)の場合、Naでは(IAファミリーからのものであるため)1つの価電子しかなく、Clでは(VIIAファミリーからのものであるため)7つの価電子が表されます。
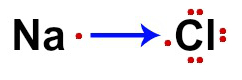
NaCl電子式
Cl(非金属)による電子の獲得とNa(非金属)による電子の喪失は矢印で表されます。 による オクテット理論、Naは1つしかないために電子を失い、Clは1つを獲得して8つの価電子を完成させます。
今やめないで... 広告の後にもっとあります;)
共有結合化合物の場合
a)分子式
分子式は、共有結合物質を簡略化した形で表すために使用されます。 Hである水の分子式2たとえば、Oには2つの水素原子と1つの酸素原子があります。
イオン性化合物のイオン式とは異なり、共有結合性化合物の分子式はそれほど多くのもので構築されていません 同じ元素の異なる量の原子が水などの異なる物質を形成するため、単純さ (H2O)および過酸化水素(H2O2).
演習では、分子式は非常に一般的です。
演習自体によって提供されます。
計算によって決定されます。
構造式から各要素を数えることによって決定されます。
物質名から決定します。
b)構造式
共有結合物質の構造式は、各原子が分子内で作る結合の数を表すために使用されます。 構造式で使用されるリンクは次のとおりです。
単一リンク:ダッシュ(─)で表され、単一リンクを示します。
二重結合:2つのダッシュ(=)で表され、2つの結合を示します。
三重結合:3つのダッシュ(≡)で表され、3つの結合を示します。
与格リンク:矢印(→)で表され、単一の接続を示します。
共有化合物の構造式は、可能な限り、問題の分子の分子構造に従って表す必要があります。 ピラミッド型の形状を持つアンモニアの構造式の表現を参照してください。
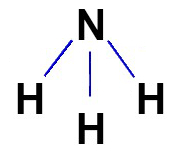
c)電子式
共有化合物の電子式は、分子を構成する原子間での電子の共有を示しています。 構造式で使用されるダッシュの代わりに、原子間で共有される電子を表すために球を使用します。 見てください:
単結合:2つの電子を共有します(関係する各原子から1つ)。
二重結合:4つの電子を共有します(関係する各原子から2つ)。
三重結合:6つの電子を共有します(関与する各原子から3つ)。
配位結合:2つの電子の共有(両方とも関係するものの間の単一の原子からのもの)、
したがって、構造式が上に表されているアンモニアの場合、その電子式は次のようになります。
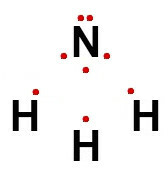
金属化合物の場合
金属化合物は、単一の金属の原子によってのみ形成されるため、化学式として化学元素の略語があります。
銅物質:Cu
金物質:Au
鉄物質:Fe
私によって。DiogoLopesDias
学校や学業でこのテキストを参照しますか? 見てください:
DAYS、ディオゴロペス。 "化学物質の処方"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/formulas-substancias-quimicas.htm. 2021年6月27日にアクセス。