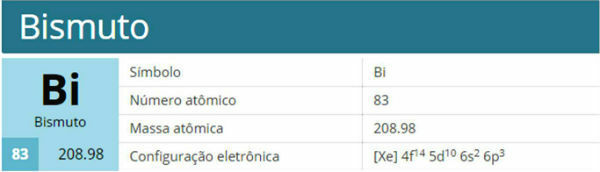
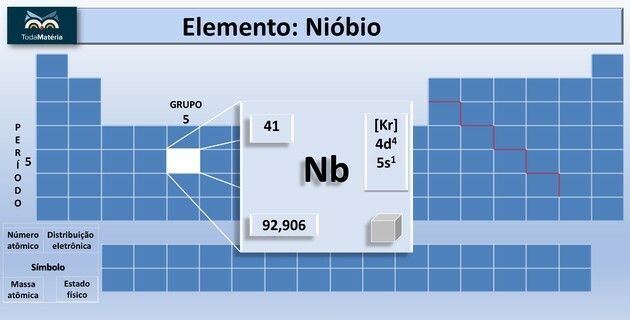
だけでなく、 サイクラン、アルケン、アルキン、 とりわけ、 アルカジエン また、電話に苦しむ 付加反応. についてのテキストで ジエンの反応、付加反応は、作業中のジエンの種類によって異なることがわかります。 ジエンは大きく次のように分類できます。
凝縮または蓄積 (2つのダブルの間に単結合はありません);
例:H2C = CH-CH3
共役または交互 (2つのダブル間の単結合のみ);
例:H2C = CH-CH = CH2
孤立 (2つのダブル間の少なくとも2つの単結合)。
例:H2C = CH-CH2-CH2—CH = CH2
ディールス・アルダー反応 1928年に2人のドイツ人化学者、オットーポールヘルマンディールスとカートアルダーによって開発されました。 これは、次のことを可能にするため、OrganicChemistry内の非常に重要な反応です。
ジエン炭化水素を特定します。
飽和環状炭化水素を得る (好ましくはシクロヘキサン)。
この有機反応はでのみ発生します アルカジエンまたは共役または交互ジエン と呼ばれます 追加1.4. より簡単な方法で1,4の付加を観察できる化合物は、ブタ-1,3-ジエンであり、以下に表されます。
H2C = CH-CH = CH2
注意:この化合物では、 共振現象、2つのパイ結合からの電子が鎖を通って移動します。 対 パイ電子 チェーンの中央領域を占有し始めます(炭素2と3の間)、他のパイ結合からの電子は末端炭素の1つにシフトします。 したがって、炭素1と4に結合部位があり、炭素2と3の間に二重の結合部位があります。

but-2,3-ジエン構造の共鳴
今やめないで... 広告の後にもっとあります;)
で ディールス・アルダー反応、 試薬の1つは共役ジエンであり、もう1つは存在する可能性のある有機化合物です。 電話 炭素原子間で2倍。 以下はの例です ディールス・アルダー反応 but-2,3-ジエンとプロペンの間:
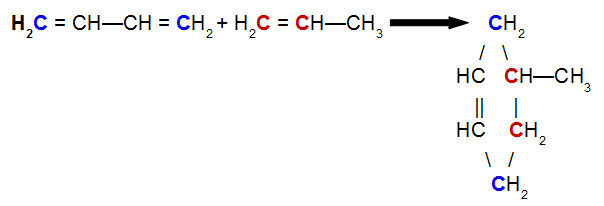
ブト-2,3-ジエンとプロペンのディールス・アルダー反応の方程式
上記の式を分析すると、but-2,3-ジエン結合の炭素1と4(両方とも青色)がわかります。 それぞれプロペンの炭素1と2(両方とも赤)になり、分岐したサイクレンを生成します。 4-メチル-シクロヘキセン。 これは、炭素2と3の間のパイ結合をシフトするbut-2,3-ジエン分子の共鳴と、プロペンの炭素1と2の間のパイ結合の切断によるものです。
OBS.²: 共役アルカジエンと反応する化合物に関係なく、鎖の炭素原子間でのみパイ結合が切断されることを強調することが重要です。 構造が炭素以外の原子間にパイ結合を持っている場合、それらは壊れません。 以下は、と反応できる構造の例です。 アルカジエン で ディールス・アルダー反応、これにより、二重結合の炭素(青色)間のパイ結合が切断されます。
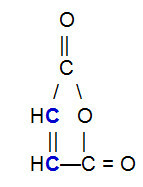
無水マレイン酸の構造式
私によって。DiogoLopesDias
学校や学業でこのテキストを参照しますか? 見てください:
DAYS、ディオゴロペス。 "ディールスアルダー反応"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/reacoes-diels-alder.htm. 2021年6月28日にアクセス。
化学

アルケン、ガス、エテン、エチレン、プラスチック、合成ゴム、染料、合成繊維、 爆発物、石油分解、ポリエチレン、油性ガス、オレフィン、炭化水素、鎖 非環式二酸化炭素。