可逆的および不可逆的プロセスの概念は、エントロピーの概念を使用して数学的に説明できます。 しかし、エントロピーの定義に入る前に、可逆的および不可逆的プロセスの概念に取り掛かりましょう。 私たちは 可逆プロセス システムが自発的に元の状況(または状態)に戻ることができるもの。 不可逆的なプロセス システムが自発的に元の状態に戻ることができないものです。
プロセスのタイプの概念についてはすでに説明したので、エントロピーの定義に進みましょう。 THE エントロピ システムの(S)は、その混乱の程度の尺度です。 組織が大きいほど、エントロピーは低くなります。 エントロピーは、内部エネルギー、体積、およびモル数と同様に、熱力学的状態の特性です。
上の図のコンテナを見ると、コンテナ1には エントロピ 他よりも小さい。 容器を持って振ると、「ボール」が混ざり合っているか、まとまりがないか確認します。 コンテナ2を振った後、チェックすると、ボールが不可能であることがわかります。 自発的に、私たちが揺れ続けるならば、彼らの元の組織に戻ります コンテナ。
可逆等温(温度が常に同じままである)可逆プロセスでは、エントロピーを温度に対する熱(与えられたまたは受け取られた)の比率として定義します。 したがって、等温プロセスのエントロピーを次のように表します。
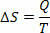
国際単位系では、ジュール/ケルビンでエントロピーを測定します。 エントロピーについて説明する概念に基づいて、次のように第2法則を定式化できます。

孤立系のエントロピー変化は常に正またはヌルです。 等式ΔS= 0は、プロセスが可逆的である場合に発生します。可逆的プロセスはエントロピーを増加させません。 環境に熱を受け取ったり与えたりしない孤立したシステムは、エントロピーを増加させるか、一定に保つことしかできません。
ドミティアーノ・マルケス
物理学を卒業
ブラジルの学校チーム
ソース: ブラジルの学校- https://brasilescola.uol.com.br/fisica/entropia-segunda-lei.htm

