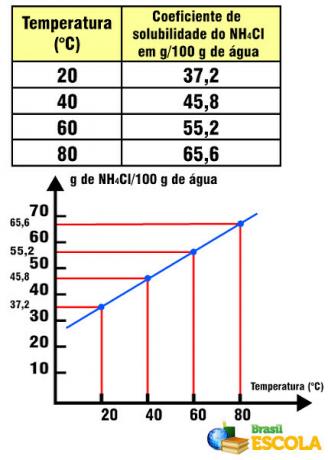
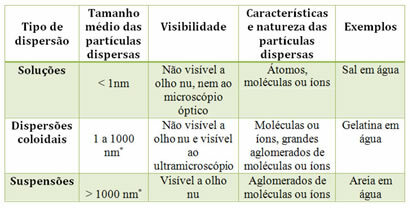
酸化反応では電子の損失が発生し、還元反応では電子の獲得が行われます。
THE 酸化 これは、酸素が物質に追加されたとき、物質が水素を失ったとき、または物質が電子を失ったときの3つの状況で発生する可能性があります。 例:フルーツサラダは、酸素が果物の酸化を促進するように作用するため、空気に触れると暗くなる傾向があります。 これが起こらないためのヒントは、柑橘系の果物に含まれるビタミンCがサラダへの酸素の酸化作用を防ぐため、レモンまたはオレンジジュースを追加することです。
THE 削減は逆であり、3つの方法で発生します。物質が酸素を失うとき、水素を得るとき、または電子を得るときです。 例:酸化銅(黒)を適切な装置(チャンバー)に入れて還元すると、水素ガスが入ります。 過熱した酸化銅と接触すると、酸素が失われ、還元されるにつれて徐々にピンク色に変わります。 銅。
酸化物還元反応:同じ化学反応で酸化と還元が同時に起こることが知られています。 この現象は 酸化還元反応または酸化還元. 酸化還元は、物質間で電子を移動させ、ある物質の酸化数(nox)を増加させ、別の物質のnoxを減少させる反応です。 このプロセスは、イオン結合(電子が1つの物質から別の物質に移動する)と混同しないでください。むしろ、ある物質の酸化と別の物質の還元のプロセスとして混同する必要があります。 この反応では、電子を失って酸化する物質を還元剤と呼び、電子を獲得して還元する物質を酸化剤と呼びます。
これらの反応のいくつかは、業界にとって非常に役立ちます。 たとえば、鉄は高炉で鉄鉱石と一酸化炭素(CO)を組み合わせて抽出されます。 この反応では、鉱石は酸素を失って鉄(Fe)を形成し、COは酸素を受け取ってCOを形成します2 (二酸化炭素)。 さびは、鉄が酸化して酸化鉄(さび)を形成し、空気中の酸素が還元される酸化還元反応の結果の1つです。
酸化還元反応の別の例は、空気と接触している銀の反応です。 銀色のオブジェクトは、時間の経過とともに光沢のある外観を失い、色がくすんで暗くなる傾向があります。 この事実は、物体の表面の銀原子が酸素などの他の物質と反応するために発生します。 次に、銀が酸化した、つまり酸化還元反応を起こしたと言います。
今やめないで... 広告の後にもっとあります;)
リリア・アルベス
化学を卒業
学校や学業でこのテキストを参照しますか? 見てください:
SOUZA、LíriaAlvesde。 "酸化と還元"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/oxidacao-reducao.htm. 2021年6月27日にアクセス。