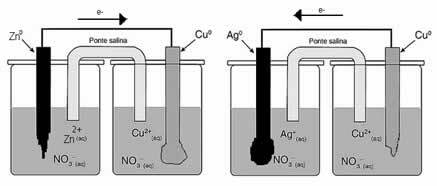
אם נשתמש במד מתח בסוללה, נוכל לזהות את ההבדל בפוטנציאל (U או ddp) או בכוח האלקטרומטיבי (emf או E) בין שתי האלקטרודות. עם זאת, לא ניתן לזהות בצורה זו את פוטנציאל ההפחתה או החמצון של כל אלקטרודה.
מדענים היו צריכים לדעת ערכים אלה כדי לחקור תהליכים להפחתת חמצון, ולכן הם הקימו א מצב התייחסות. פירוש הדבר שהוסכם על מדידת הפוטנציאל של כל אלקטרודה ביחס לאלקטרודה אחרת בתנאים הסטנדרטיים הבאים:
• הטמפרטורה חייבת להיות 25 מעלות צלזיוס;
• לחץ ב 1.0 atm;
• ריכוז התמיסה בה טובלת המתכת חייב להיות 1.0 mol / L.
לפיכך, האלקטרודה שנבחרה הייתה אלקטרודת מימן, המיוצג להלן:
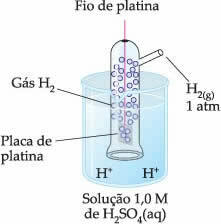
אלקטרודה זו מורכבת מחוט פלטינה המחובר לצלחת פלטינה, שאינו משתתף בתגובה, בתוך צינור המכיל גז מימן ושקוע בתמיסה חומצית. בדוגמה, הפתרון היה חומצה גופרתית.
| לפי ההסכם, האלקטרודה המימנית הסטנדרטית הוקצתה לערך אֶפֶס, כל כך הרבה ל- E0אָדוֹם באשר ל- E.0אוקסי. |
לפיכך, כדי למצוא את הערך הפוטנציאלי של כל אלקטרודה אחרת, אנו פשוט בונים ערימה של האלקטרודה שאנו רוצים עם אלקטרודת המימן הסטנדרטית ונמדוד את ה- ddp בעזרת מד מתח. הערך המוצג במד המתח יהיה הפוטנציאל של האלקטרודה המבוקשת, מכיוון שמימן שווה לאפס.
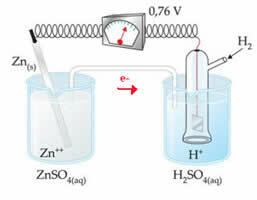
לדוגמא, אנו מקשרים בין אלקטרודת אבץ לבין אלקטרודת המימן כדי לגלות מהו פוטנציאל ההפחתה שלה:
אל תפסיק עכשיו... יש עוד אחרי הפרסום;)
על פי התוכנית לעיל, מד המתח זיהה את ההפרש הפוטנציאלי כשווה ל- +0.76 (? E0 = +0.76). נציין גם כי אלקטרודת האבץ התחמצנה, כך שהיא האנודה; ואלקטרודת המימן הופחתה, בהיותה הקתודה.
אז יש לנו:
? E0 = E0red (קתודה) - E0 אדום (אנודה)
0.76 = 0.00 - E0 אדום (Zn)
E0 אדום (Zn) = 0.00-0.76
E0 אדום (Zn) = -0.76
הערך השלילי פירושו שזרם האלקטרון זורם מאלקטרודת האבץ (האנודה) לאלקטרודת המימן, וכך מתנהג כמו קתודה. אם זה היה חיובי, זה היה הפוך, ואלקטרודת המימן תתנהג כמו אנודה. ניתן לראות זאת כאשר אנו מחברים בין אלקטרודת נחושת לבין אלקטרודת המימן הרגילה:
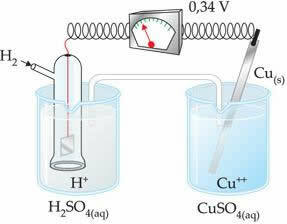
? E0 = E0red (קתודה) - E0 אדום (אנודה)
-0.34 = 0.00 - E0 אדום (Zn)
E0 אדום (Zn) = 0.00 + 0.34
E0 אדום (Zn) = +0.34
לפיכך, ניתן להגדיר את פוטנציאל ההפחתה והחמצון עבור המינים הכימיים המגוונים ביותר. עם זאת, האיגוד הבינלאומי לכימיה טהורה ויישומית (IUPAC) ממליץ על שימוש בפוטנציאל הפחתה בלבד. וללא קשר למתכת המשמשת, בייצוג הסוללה, אלקטרודת המימן תמיד באה במקום הראשון, למשל:
Pt - H2 (g) 1atm / H3O1 + (aq) 1 mol / L // Cu2 + (aq) 1 mol / L / Cu
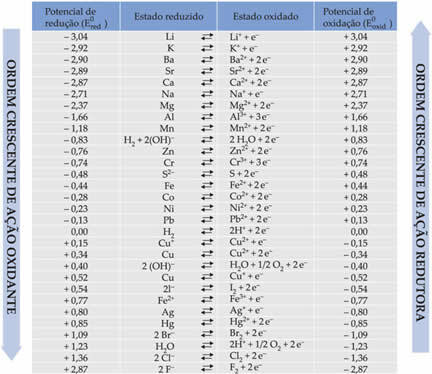
להלן הטבלה מציגה את הפוטנציאלים המושגים באמצעות שיטה זו של שימוש באלקטרודת המימן הסטנדרטית, יחד עם חצי התגובות שלהם בהתאמה:
מאת ג'ניפר פוגאצה
בוגר כימיה
צוות בית הספר בברזיל
האם תרצה להתייחס לטקסט זה בבית ספר או בעבודה אקדמית? תראה:
FOGAÇA, ג'ניפר רושה ורגס. "מדידת פוטנציאלים אלקטרוכימיים"; בית ספר ברזיל. אפשר להשיג ב: https://brasilescola.uol.com.br/quimica/medicao-dos-potenciais-eletroquimicos.htm. גישה אליו ב -28 ביוני 2021.