ה אלקטרוכימיה הוא ענף של כימיה פיזיקלית החוקרת את התגובות בהן יש העברת אלקטרונים (תגובות צמצום אוקסי) ותגובותיה המרה לאנרגיה חשמלית, כמו גם תהליך הפוך, כלומר המרת אנרגיה חשמלית לאנרגיה כִּימִיָה.
התהליך הראשון הוא המתרחש ב סוללות. סוללות הן מכשירים שנוצרים על ידי שתי אלקטרודות (קוטב חיובי, שהוא הקתודה, וקוטב שלילי, שהוא האנודה), בנוסף לאלקטרוליט (פתרון מוליך). אלקטרונים מועברים על ידי מוליך חיצוני מהאנודה לקתודה, ויוצרים זרם חשמלי המשמש להפעלת מכשיר כלשהו. הסוללות מורכבות מכמה תאים המחוברים בסדרה או במקביל.
זהו תהליך ספונטני ואנרגיה מסופקת עד למיצוי התגובה הכימית (כמו במקרה של תאים וסוללות ראשוניים, כמו התא היבש של לקלאנשה והסוללה. אלקליין), או, במקרה של תגובות הפיכות, ניתן ליישם הבדל פוטנציאלי ולהפוך את התגובה, ליצור שוב את המגיבים ולהטעין את הסוללה ש מוכן לשימוש שוב (זה המקרה של סוללות וסוללות משניות, כגון עופרת, המשמשות במכוניות וליון יון המשמשות במכשירים טלפון נייד).

תאים ראשוניים וסוללות בחזית ובשניה טעינה של סוללות משניות (עופרת וליון ליתיום)
התהליך ההפוך אינו ספונטני ונקרא הַפרָדָה חַשְׁמָלִית
. אלקטרוליזה היא מעבר זרם חשמלי המגיע מגנרטור, כגון תא או סוללה, דרך נוזל יוני. אם הנוזל הוא חומר מותך כלשהו, יש לנו אלקטרוליזה דלקתיתאבל אם זה פיתרון מימי, יש לנו אלקטרוליזה מימית.כאשר מעבירים את הזרם החשמלי על המדיום הנוזל, הגנרטור "מושך" את האלקטרונים מהקוטב החיובי (אנודה - הוא ההפך מזה סוללה) של התא האלקטרוליטי ומעביר אותם לקוטב השלילי (קתודה), כלומר הקתודה עוברת צמצום והאנודה עוברת חִמצוּן. לפיכך, האנרגיה החשמלית שמספק הגנרטור הופכת לתגובות חיזור (אנרגיה כימית). להלן תוכנית אלקטרוליזת מים:
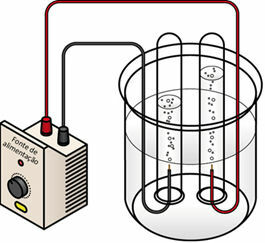
תוכנית אלקטרוליזת מים
אלקטרוליזה מיושמת באופן נרחב בתעשייה בייצור חומרים חשובים, כגון אלומיניום, גז כלור, נתרן מתכתי, וכדי לטהר או להגן על מתכות שונות, כמו בתהליכי גלוון או גלוון, הכוללים ציפוי של חפץ כלשהו על ידי מתכת, כגון הכסף, ציפוי נחושת, ציפוי ניקל, הזהבה ו כרומציה; כאשר פלדה מצופה באבץ, זה נקרא גלוון.
בחלק של אלקטרוכימיה באתר האינטרנט שלנו תוכלו למצוא פרטים נוספים על כל ההיבטים הקשורים לתאים ולסוללות, כמו גם אלקטרוליזה.
מאת ג'ניפר פוגאצה
בוגר כימיה
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-eletroquimica.htm
