לימודי כימיה חשובים והטרנספורמציות שהיא עוברת. החומר, בתורו, הוא כל מה שתופס מקום במרחב ולכן יש לו מסה ונפח. ניתן למצוא אותו בשתי דרכים בסיסיות: חומרים ו תערובות.
כמוסבר בטקסט “מהו חומר?", חומר מוגדר כאשר חומר נתון נוצר רק על ידי סוג אחד של רכיב (שיכול להיות חלקיקים כמו אטומים, מולקולות, נוסחאות יחידה, אלקטרונים או יונים), וכתוצאה מכך, יש להם תכונות פיזיקליות כגון נקודת התכה, נקודת רתיחה וצפיפות, קבועות וטובות. מוּגדָר.
כְּבָר תערובות הן מערכות הנוצרות על ידי שני חומרים מורכבים או יותר או פשוטים שונים. באופן זה הם מציגים תכונות פיזיקליות לא מוגדרות ומשתנות. מאפיינים אלה תלויים בכמות כל חומר בתערובת ואופיים.
מפת חשיבה: תערובות
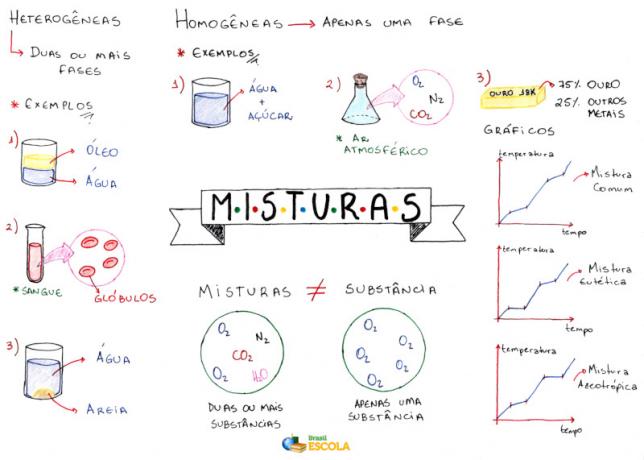
* להורדת מפת החשיבה ב- PDF, לחץ כאן!
לדוגמא, האלכוהול האתילי הנפוץ בו אנו משתמשים לניקוי וחיטוי אינו חומר טהור, מכיוון שהוא אינו מורכב רק ממולקולות אתנול (H3C-CH2-או). כפי שמציין התווית על הבקבוק של מוצר זה, מדובר בתערובת של אתנול ומים (H2O). לדוגמה, אם אתה רואה על התווית כי האלכוהול הוא בריכוז של 96ºGL (מעלות גיי-לוסאק), המשמעות היא שבמאה חלקים של תערובת זו, ישנם 96 חלקי אתנול ו -4 חלקי מים, כלומר בקבוק של 100 מ"ל אלכוהול מיובש מכיל 96 מ"ל אתנול ו -4 מ"ל מים.
ניתן לסווג תערובות ל הוֹמוֹגֵנִי ו הֵטֵרוֹגֵנִי. במקרה של אלכוהול מיובש, יש לנו תערובת הומוגנית. אך מהי תערובת הומוגנית? זו תערובת שבה איננו יכולים לראות את ההפרדה בין מרכיביה. אורכו אחיד ובעל שלב יחיד.
תערובות הומוגניות אלה נקראות גם פתרונות, כאשר החלקיקים המפוזרים בקוטר קטן מ -1 ננומטר, כלומר, אפילו לא באמצעות אולטרה מיקרוסקופ ניתן לראות יותר משלב אחד בחומרים אלה. יתר על כן, לא ניתן להפריד בין מרכיביו בשיטות פיזיקליות כגון צנטריפוגות או סינון.
דם הוא תערובת. בעין בלתי מזוינת זה נראה כאילו מדובר בתערובת הומוגנית, אך לא כך, כי מתחת למיקרוסקופ אנו רואים את מרכיביו. יתר על כן, כאשר מציבים אותו בצנטריפוגה, מרכיבים אלה מופרדים.

דם צנטריפוגה ותדמיתו במיקרוסקופ
תערובות או פתרונות הומוגניים יכולים להיות בכל שלושת המצבים הפיזיים. האלכוהול המוזכר שהוזכר הוא דוגמה ל תערובת נוזלית. אוויר הוא תערובת גז המורכב מכמה גזים, העיקריים הם חנקן (N2) וחמצן (O2). סגסוגות מתכת הן תערובות מוצקות, כגון פלדה המורכבת מכ- 98.5% Fe (ברזל), 0.5 עד 1.7% C (פחמן) ועקבות של Si (סיליקון), S (גופרית) ו- P (זרחן).
בְּ תערובות הטרוגניות, מצד שני, הם אלה שיש להם יותר משלב אחד, כמו ערבוב מים ושמן, מים וחול, גרניט (תערובת של קוורץ, נציץ ופלדה ספא) וכן הלאה.

דוגמה לתערובת הטרוגנית תלת פאזית
כאמור, התכונות הפיזיקליות של התערובות אינן קבועות ולא נקבעות. עם זאת, ישנם תערובות מסוימות שהן יוצאות מהכלל, התערובות אזוטרופיות ו eutectic. לתערובות אזוטרופיות יש נקודת רתיחה או עיבוי קבועים, כשהם מתנהגים, באותה נקודה, כחומר טהור.. האלכוהול 96% שהוזכר הוא תערובת אזוטרופית מכיוון שיש לו נקודת רתיחה קבועה ב 78.2 מעלות צלזיוס.
עכשיו כן, תערובות eutectic הם אלה שמתנהגים כאילו היו חומר טהור רק במהלך ההתמצקות או נקודת ההיתוך. דוגמה לכך היא סגסוגת מתכתית העשויה מקדמיום 40% וביסמוט 60%, אשר נקודת התכה קבועה שווה ל -140 מעלות צלזיוס.
אך הרוב המכריע של התערובות משנה את מצבן הפיזי לא בטמפרטורה קבועה, אלא בטווחי טמפרטורה לא ספציפיים.
מפה נפשית מאת האם ויקטור ריקרדו פריירה
מורה לכימיה
מאת ג'ניפר פוגאצה
בוגר כימיה
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-uma-mistura.htm