אחד האתגרים הגדולים ביותר עבור כל מי שלומד כימיה נקרא הפצה אלקטרונית. מה שאנחנו הולכים להציג בהקשר זה יכול להקל מאוד על הלימודים שלך הקשורים לתצורת האלקטרונים שהציע המדען לינוס פאולינג.
המספר המרבי של אלקטרונים שמתאים לכל שכבה או רמת אנרגיה ניתן דרך הטבלה:
שכבת רמת האנרגיה מספר אלקטרונים מקסימלי
1 K 2
2 L 8
3 M 18
רביעי N 32
5 ° O 32
6 P 18
ש '8
סדר האנרגיה ההולך וגדל של תת-הגבולות הוא הסדר ברצף האלכסונים. התרשים של לינוס פאולינג מוצג להלן:
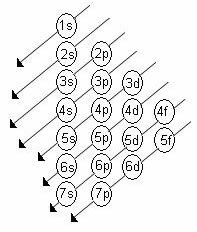
כללים בסיסיים:
1. המספר האטומי (Z) של היסוד, במצב ניטרלי, מציין את מספר האלקטרונים להפצה. מספר זה מיוצג בחלק השמאלי התחתון של סמל האלמנט.
2. בעזרת דיאגרמת פאולינג התחל לחלק את האלקטרונים מלמעלה למטה, תוך התחשבות בסדר האנרגיה ההולך וגדל (מכוון לפי כיוון החצים).
3. מלא את רמת המשנה ברמת האלקטרונים המקסימלית. אם רמת משנה נתונה מחזיקה רק 6 אלקטרונים, אל תחרוג מכמות זו.
4. בדוק את מספר האלקטרונים על ידי הוספתם בכל תת-משנה.
בואו נבצע את זה בפועל?
הפץ את האלקטרונים של אטום הברזל (Z = 26).
אם המספר האטומי הוא 26, המשמעות היא שבאטום הברזל הרגיל יש 26 אלקטרונים. החלת דיאגרמת פאולינג תהיה לנו:

מאת ליריה אלבס
בוגר כימיה
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/quimica/regras-distribuicao-eletronica.htm
