אטום הפחמן נחשב מיוחד בזכות יכולתו ליצור קשרים עם אטומים אחרים ולהוליד שרשראות פחמן ארוכות. הכל נובע מהטטרוולנציה של הפחמן, הוא יכול להצטרף וליצור ארבעה קשרים, והאטומים המשתתפים יכולים להיות פחמן או אלמנטים אחרים. האחרונים, כאשר הם נמצאים בשרשרת הפחמן, נקראים הטרואטומים.
ההטרואטומים הנפוצים ביותר הם: חנקן (N), חמצן, גופרית (S) וזרחן (P).
דוגמא:
אטום החמצן הקיים בשרשרת שלמעלה הוא הטרו-אטום, כפי שהוא בין פחמנים.
אבל היזהר! אל תבלבל הסתעפות עם פחמן הטרואטום, ראה:
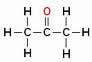
אטום החמצן (באדום) אינו ממוקם בין פחמנים אלא מעליהם, ויוצר ענף, ולכן הוא לא יכול להיחשב כהטרו-אטום.
סיווג אטומים בשרשרת פחמן:
בשרשרת, כל פחמן מסווג לפי מספר אטומי הפחמן האחרים המחוברים אליו.
פחמן ראשוני: מחובר ישירות לפחמן אחד נוסף בלבד.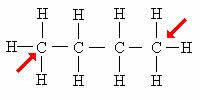
החץ מציין את הפחמנים הראשוניים. שים לב כי מכיוון שהם ממוקמים בקצות שרשרת הפחמן, אטומים אלה נקשרים לפחמן אחד בלבד.
פחמן משני: מקושר ישירות לשני פחמנים אחרים.
הפחמנים המצוינים ממוקמים בין שני פחמנים.
פחמן שלישוני: מקושר ישירות לשלושה פחמנים אחרים.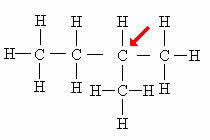
שים לב שנוכחות הענף (CH3) המחובר לאטום המצוין גורם לו לקבל את סיווג הפחמן השלישוני.
פחמן רביעי: מקושר ישירות לארבעה פחמנים אחרים.
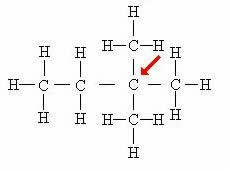
במקרה זה, ארבעת האטומים המחוברים לפחמן המרכזי (המצוין על ידי החץ) יוצרים מעין "ריבוע", המעיד עוד יותר על הימצאות הפחמן הרבעוני.
מאת ליריה אלבס
בוגר כימיה
צוות בית הספר בברזיל
ראה עוד!
סיווג שרשראות פחמן: סוגי קשר
תכונות של תרכובות אורגניות
כימיה אורגנית - כִּימִיָה - בית ספר ברזיל
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/quimica/capacidade-compostos-organicos-formar-cadeias.htm
