מלחים אנאורגניים הם נוצרים על ידי האגודה היונית של לפחות קטיון אחד (שנוצר על ידי מתכת כלשהי או על ידי אמוניום) ואניון (פשוט או תרכובת).
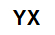
נוסחה מולקולרית כללית של מלח
כאשר מוסיפים אותם למים, המלחים מתנתקים, ומשחררים לפחות קטיון אחד שאינו הידרוניום (H+) ואניון שאינו הידרוקסיד (OH-).
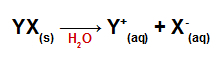
משוואת דיסוציאציה לכל מלח
סיווג מלחים
מלחים, באופן כללי, יכולים לקבל את הסיווגים הבאים:
מלח פשוט: מלח שנוצר על ידי קטיון אחד ואניון אחד בלבד. דוגמאות: NaCl, CaSO4, KCN, NH4שיתוף3 וכו '
מלח מיוצר: יש לו שני קטיונים (אחד מהם חייב להיות הידרוניום) ואניון. דוגמאות: NaHCO3, CaHBO3 וכו '
מלח הידרוקסיל: יש לו קטיון ושני אניונים (אחד מהם חייב להיות ההידרוקסיד). דוגמאות: MgOHCl, Al (OH)2ClO3 וכו '
מלח מיובש: מציג מולקולות מים הקשורות למבנה הגבישי שלה. דוגמאות: CaCl2.2H2O, CuSO4.6H2וכו '
מלח כפול: יש לו שני קטיונים (כולם שונים מהידרוניום) ואניון אחד או קטיון אחד ושני אניונים (כולם שונים מהידרוקסיד). דוגמאות: סוג4CN, AgFeBO3 וכו '
אלום: הוא המלח שנוצר על ידי שני סולפטים עם קטיונים של NOx השווים ל- +1 ו- +3, בתוספת 24 מולקולות מים. דוגמאות: Ag2רק4.אל2(רק4)3.24H2על2רק4.Sb2(רק4)3.24H2או
כלל שמות מלח
שם אניון + שם + קטיון
→ K3אָבָק4
במלח יש את האניון הפוספט (PO4-3) וקטיון האשלגן (K+1ומכאן שמו שמו אשלגן פוספט.
→ מקרה3
במלח יש את האניון הסולפיט (SO3-2) וקטיון הסידן (Ca+2ומכאן ששמו הוא סידן גופרתי.
הערה: אם הקטיון אינו כסף, אבץ או אלמנט השייך למשפחות IA, IIA ו- IIIA, עלינו לציין את ה- NOX שלו עם ספרה רומאית מול שם הקטיון.
→ Cu2רק4
במלח יש את האניון הגופרתי (SO4-2) וקטיון הסידן (Cu+1ומכאן שמו נחושת סולפט I.
מלח מיוצר: עבור מלח זה, לפני שם האניון, עלינו לכתוב את הקידומת המתייחסת לכמות המימן בנוסחה. קידומת זו חייבת להיות נפרדת מהמילה מֵימָן על ידי מקף.
→ NaHCO3
במלח יש מימן, אניון פחמתי וקטיון נתרן, אז שמו הוא נתרן חד מימן פחמתי.
מלח הידרוקסיל: עבור מלח זה, לפני שם האניון, עלינו לכתוב את הקידומת המתייחסת לכמות ההידרוקסילים בנוסחה. קידומת זו חייבת להיות נפרדת מהמילה הידרוקסי על ידי מקף.
→ אל (אוה)2ClO3
במלח שני הידרוקסילים, אניון הכלוראט וקטיון האלומיניום, כך ששמו אלומיניום דיהידרוקסי-כלור.
מלח מיובש: עבור מלח זה, על שם הקטיון, עלינו לכתוב את הקידומת המתייחסת לכמות מולקולות המים בנוסחה. קידומת זו חייבת להיות נפרדת מהמילה מיובש על ידי מקף.
→ CaCl2.2H2או
במלח יש שתי מולקולות מים, האניון הכלורי והקטיון הסידן, ולכן שמו הוא סידן כלורי.
מלח כפול עם שני קטיונים: עבור מלח זה, עלינו לכתוב את המילה הכפולה בסוגריים אחרי שם האניון ואז את שם הקטיון האלקטרו-חיובי ביותר ואת הקטיון השני.
→ AgFeBO3
במלח זה יש כסף (קטיון אלקטרופוזיטיווי יותר) וקטיון ברזל II, בנוסף לאוניון הבוראט. שמו בוראט (כפול) מכסף וברזל II.
-
מלח כפול עם שני אניונים:
שם האניון האלקטרוני שלילי + מקף + שם האניון האלקטרוני שלילי + שם הקטיון
→ סוּג4CN
מלח זה מכיל את קטיון IV טיטניום, בנוסף לפוספט (אניון אלקטרוני יותר) ואניון ציאניד. שמו הוא טיטניום פוספט ציאניד IV.
מלח אלום: לגבי מלח זה, אנו מתעלמים מהכלל הכללי. פשוט כתוב את המונח אלום ואחריו שם קטיון המטען +3 ושם קטיון המטען +1 בהתאמה, מופרדים בצירוף e.
→ ב2רק4.Sb2(רק4)3.24H2או
במלח האלום יש את קטיון האנטימון +3 ואת קטיון הנתרן +1, ולכן שמו הוא אלום ונתרן אנטימון III.
מאפיינים פיזיים של מלחים
הם מוצקים בטמפרטורת החדר;
יש להם נקודות התכה ורתיחה גבוהות;
הם נוצרים מקשרים יוניים;
הם מוליכים זרם חשמלי במצב נוזלי (לאחר שעברו מיזוג) או כשהם מומסים במים;
באופן כללי, הם מסיסים במים, אך ישנם מלחים הנחשבים למסיסים כמעט.
תכונות כימיות של מלחים
מלחים הם תרכובות בעלות יכולת תגובה כימית (בתנאי שאין להם אותו קטיון או אותו אניון כמו חומר אחר) עם מספר קבוצות של חומרים, כלומר:
בתגובה חילופית כפולה עם חומצה: הם יוצרים מלח חדש וחומצה חדשה.
בתגובה חילופית כפולה עם בסיס: הם יוצרים מלח חדש ובסיס חדש.
ב תגובת חילוף כפולה עם מלח אחר: יוצרים שני מלחים חדשים.
יש מלחים בעלי יכולת לסבול הִתפָּרְקוּת כאשר הם נתונים לחום, ויוצרים שני חומרים חדשים או יותר. אם נחמם את הנתרן ביקרבונט (NaHCO3), למשל, הוא יתפרק ויוצר נתרן פחמתי (Na2שיתוף3), מים (ח2O) ופחמן דו חמצני (CO2).
על ידי. דיוגו לופס דיאס
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-sao-sais-inorganicos.htm
