א החוק השני של התרמודינמיקה מכתיב אילו תנאים קיימים עבור חוֹם להמיר לעבודה במנועי חום ומקררים. הוא מתייחס גם להגדרה של אנטרופיה כתופעה המסוגלת למדוד את חוסר הארגון של חלקיקים במערכות פיזיקליות.
קראו גם: קלורימטריה - ענף הפיזיקה החוקר חילופי חום
סיכום על החוק השני של התרמודינמיקה
החוק השני של התרמודינמיקה מיוצג על ידי הצהרות קלאוזיוס וקלווין-פלנק.
הצהרת קלאוזיוס עוסקת בזרימת החום מהגוף החם יותר לגוף הקר יותר.
הצהרת קלווין-פלנק מתייחסת לחוסר היכולת של מכשירים תרמיים להמיר את כל החום שלהם עֲבוֹדָה.
החוק השני של התרמודינמיקה מיושם על מנועי חום ומקררים.
מחזור קרנו הוא מחזור היעילות המקסימלי המתקבל על ידי מנועי חום.
למחזור קרנו ארבעה שלבים, התרחבות איזוטרמית הפיכה, התרחבות אדיאבטית הפיכה, דחיסה איזוטרמית הפיכה ודחיסה אדיאבטית הפיכה.
משפט קרנו מתייחס לתשואה של מכונות קרנו.
מהו החוק השני של התרמודינמיקה?
החוק השני של התרמודינמיקה הוא א חוק המתייחס לאילוצים המתרחשים בתהליכים תרמודינמיים. הוא הובע על ידי הפיזיקאים רודולף קלאוזיוס (1822-1888), לורד קלווין (1824-1907) ומקס פלאנק (1858-1947), כפי שנראה להלן:
הפיזיקאי והמתמטיקאי רודולף קלאוזיוס קבע שזרימת ההולכה של חום מתרחשת מהגוף בטמפרטורה גבוהה יותר לגוף בטמפרטורה נמוכה יותר. טמפרטורה נמוכה יותר, לכן, זה לא טבעי שהתהליך ההפוך יתרחש, לכן, יש צורך לבצע עבודה על זה מערכת. עם זה הוא קבע:
אי אפשר לבצע תהליך שהשפעתו היחידה היא העברת חום מגוף קר יותר לגוף חם יותר.|1|
הפיזיקאי המתמטי ויליאם תומסון, המכונה לורד קלווין, יחד עם תרומותיו של הפיזיקאי מקס פלאנק, ציין את חוסר האפשרות של מכשירים תרמיים בעלי יעילות של 100%, שכן תמיד יהיה איבוד חום.
יישומים של החוק השני של התרמודינמיקה
החוק השני של התרמודינמיקה מיושם על מנועי חום ומקררים.
החוק השני של התרמודינמיקה במכונות תֶרמִי
אל ה מכונות תרמיות מסוגלים להמיר חום לעבודה. מקור חם מספק חום למנוע החום, מה שהופך אותו לעבודה. שאר החום שהוא שולח למקור הקור, כפי שמתואר בתמונה למטה:
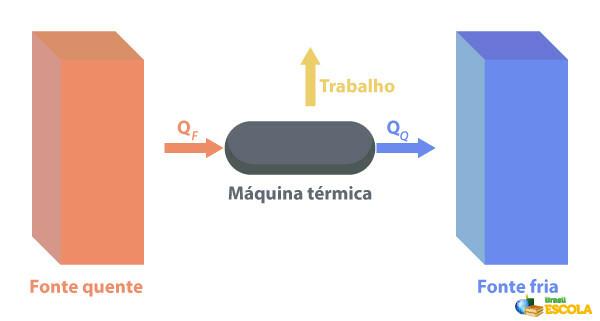
כמה דוגמאות למכונות תרמיות הן: טורבינות קיטור ונפט במטוסי סילון, מנועי בעירה, כורים תרמו-גרעיניים.
החוק השני של התרמודינמיקה במקררים
מקררים הם מכונות ש הם פועלים בצורה הפוכה לחימום מנועים., שבו הם מסירים חום מאזור עם טֶמפֶּרָטוּרָה טמפרטורה נמוכה יותר ומספקת אותה לאזור עם טמפרטורה גבוהה יותר. מכיוון שזה לא טבעי, יש צורך שהמכונה תבצע עבודה באמצעות אנרגיה חשמלית, כמתואר בתמונה למטה:
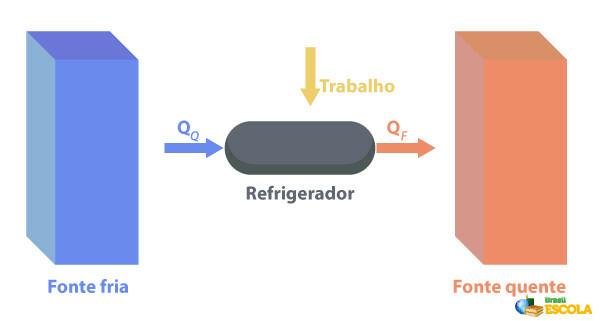
כמה דוגמאות למקררים הם מקררים ומזגנים.
אנטרופיה והחוק השני של התרמודינמיקה
א החוק השני של התרמודינמיקה מציע את קיומה של אנטרופיה, אחד כמות פיסית אחראי על מדידת מידת חוסר הארגון של חלקיקים במערכת פיזיקלית או מידת הבלתי הפיך של תהליכים תרמודינמיים המעורבים במנועי חום, בהיותם ספונטני, בלתי נמנע, בלתי הפיך ו נרחב. בכך ניתן רק לצפות ולהכיל את מידת התנודתיות של התהליכים. ככל שהאנטרופיה גדלה, עולה גם מידת האי-סדר במערכת.
א נומנקלטורית האנטרופיה היא ממקור יווני ומשמעותה "טרנספורמציה"., "שינוי", ובכך משמש ב- גוּפָנִי להצביע על אקראיות ואי-סדר. ניתן לחשב אנטרופיה באמצעות הנוסחה:
\(∆S=\frac{∆U}T\)
\(∆S\) הוא שינוי האנטרופיה, הנמדד ב-[J/K].
\(∆U\) הוא השינוי באנרגיה הפנימית, הנמדד בג'ול [J].
T היא הטמפרטורה, הנמדדת בקלווין [K].
מנקודת מבט סטטיסטית, האנטרופיה מחושבת על ידי הנוסחה:
\(S=k\cdot ln\ Ω\)
S היא האנטרופיה, הנמדדת ב-[J/K].
k הוא קבוע בולצמן, הוא שווה \(1,4\cdot 10^{-23}\ J/K\).
Ω הוא מספר המיקרו-מצבים האפשריים עבור המערכת.
קראו גם: תהליכי התפשטות חום
נוסחאות של החוק השני של התרמודינמיקה
מכונות תרמיות ומקררים
\(Q_Q=W+Q_F\)
\(Q_Q\) הוא החום של המקור החם, נמדד בג'ול [J].
W היא העבודה שמבצע מנוע החום, נמדדת בג'ול [J].
\(Q_F\) הוא החום ממקור הקור, נמדד בג'ול [J].
זה יכול להיות מיוצג על ידי:
\(W=Q_Q-Q_F\)
W היא העבודה שמבצע מנוע החום, נמדדת בג'ול [J].
\(Q_Q\) הוא החום של המקור החם, נמדד בג'ול [J].
\(Q_F\) הוא החום ממקור הקור, נמדד בג'ול [J].
מקררים
\(η=\frac{Q_F}{Q_Q-Q_F}\)
\(η\) היא היעילות של המקרר.
\(Q_F\) הוא החום ממקור הקור, נמדד בג'ול [J].
\(Q_Q\) הוא החום של המקור החם, נמדד בג'ול [J].
זה יכול להיות מיוצג כ:
\(η=\frac{Q_F}W\)
\(η\) היא היעילות של המקרר.
\(Q_F\) הוא החום ממקור הקור, נמדד בג'ול [J].
W היא העבודה שמבצע מנוע החום, נמדדת בג'ול [J].
דוגמאות של יישום נוסחאות
דוגמה 1: חשבו את העבודה שעושה מנוע חום במהלך מחזור שמקבל 500 J חום מהמקור החם ומעביר רק 400 J חום למקור הקר.
כדי לחשב את העבודה של מנוע חום, נשתמש בנוסחה:
\(W=Q_Q-Q_F\)
החלפת הערכים המצוינים בהצהרה:
\(W=500-400\)
\(W=100\ J\)
עבודתו של מנוע החום הייתה 100 ג'ול.
דוגמה 2: מהי היעילות של מקרר שמקבל 150 J חום מהמקור החם ומעביר 50 J חום למקור הקר?
כדי לחשב את היעילות של מקרר, נשתמש בנוסחה:
\(η=\frac{Q_F}{Q_Q-Q_F}\)
בהחלפת הערכים שניתנו בהצהרה, נקבל:
\(η=\frac{50}{150-50}\)
\(η=\frac{50}{100}\)
\(η=0,5\)
הכפלת התשואה ב-100%:
\(η=0.5\cdot100%\)
\(η=50\%\)
המקרר בעל יעילות של 50%.
מחזור קרנו
מחזור קרנו היה פותח על ידי המדען סאדי קרנו (1796-1832), במטרה לזהות את היעילות המקסימלית אליה ניתן להגיע באמצעות מנוע תרמי הפועל בין מקור חם למקור קר.
בהתבסס על מחקריו, קרנו זיהה שכדי להשיג את היעילות המקסימלית ממנוע חום, הוא כן הכרחי כדי שהתהליך שלו יהיה הפיך, אז הוא פיתח את מחזור התשואה המקסימלי שנקרא מחזור של קרנו, וה מנוע החום שפועל דרכו נקרא מנוע חום קרנו.. מכיוון שמחזור קרנו הפיך, ניתן להפוך אותו, וכך פותחו המקררים.
מחזור קרנו, ללא קשר לחומר בו נעשה שימוש, מורכב מארבעה תהליכים המתוארים בגרף הלחץ לפי נפח (p×V), כפי שאנו יכולים לראות בתמונה למטה:
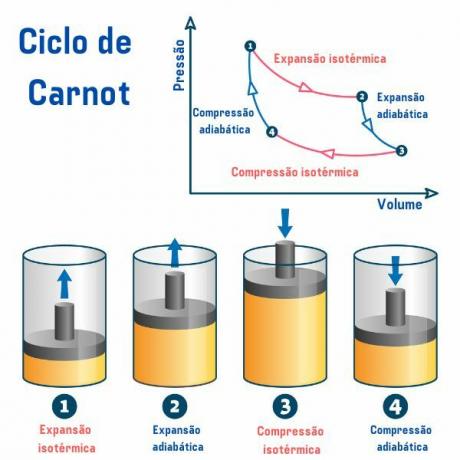
תהליך ראשון, מנקודה 1 → 2: יש התפשטות איזותרמית הפיכה (תהליך שבו הטמפרטורה נשארת קבועה), שבה הגז (או המערכת) אכן עובד ורוכש כמות חום מהמקור החם.
תהליך שני, מנקודה 2 → 3: יש התפשטות אדיאבטית (תהליך שבו יש חילופי חום עם הסביבה החיצונית) הפיכה, שבה אין חילופי חום חום עם מקורות תרמיים, אבל הגז כן עובד ויש ירידה באנרגיה הפנימית שלו, מה שגורם לירידה ב טֶמפֶּרָטוּרָה.
תהליך שלישי, מנקודה 3 → 4: מתרחשת דחיסה איזותרמית הפיכה, שבה הגז מקבל עבודה ומוותר על כמות חום למקור הקור.
תהליך רביעי, מנקודה 4 → 1: מתרחשת דחיסה אדיבטית הפיכה, שבה לא מתרחש חילופי חום עם המקורות התרמיים והגז הוא מחומם עד שהוא מגיע לטמפרטורת המקור החם, ובכך להיות במגע איתו, מסיים את מחזור.
חוקי התרמודינמיקה
חוקי התרמודינמיקה הם ארבעה חוקים השולטים בלימוד כולו תֶרמוֹדִינָמִיקָה, למד את הקשרים בין נפח, טמפרטורה ולחץ וכמויות פיזיקליות אחרות, כגון חום ואנרגיה.
חוק האפס של התרמודינמיקה: הוא החוק של איזון תרמי, הוא חוקר את חילופי החום בין גופים שיש להם טמפרטורות שונות.
החוק הראשון של התרמודינמיקה: הוא חוק שימור האנרגיה במערכות תרמודינמיות, הוא חוקר את הפיכת החום לעבודה ו/או לאנרגיה פנימית.
החוק השני של התרמודינמיקה: זה החוק שעוסק במנועי חום, מקררים ואנטרופיה.
החוק השלישי של התרמודינמיקה: הוא החוק של אפס מוחלט, היא חוקרת את ההשפעות של הטמפרטורה הזו.
קרא גם: ביצועים של מנועי חום
פתרו תרגילים על החוק השני של התרמודינמיקה
שאלה 1 קבעו את טמפרטורת המקור החם של מנוע קרנו, בידיעה שטמפרטורת המקור הקר היא 450 K ויעילותו היא 80%.
א) 2250K
ב) 450K
ג) 1500K
ד) 900K
ה) 3640K
פתרון הבעיה:
חלופה א'. נחשב את הטמפרטורה של המקור החם על סמך נוסחת היעילות של מנוע קרנו:
\(η=1-\frac{T_F}{T_Q} \)
\(80 \%=1-\frac{450}{T_Q} \)
\(\frac{80}{100}=1-\frac{450}{T_Q} \)
\(0,8=1-\frac{450}{T_Q} \)
\(0,8-1=-\frac{450}{T_Q} \)
\(-0,2=-\frac{450}{T_Q} \)
\(0,2=\frac{450}{T_Q} \)
\(T_Q=\frac{450}{0,2}\)
\(T_Q=2250\ K\)
שאלה 2 (Cefet-PR) ניתן לומר את העיקרון השני של התרמודינמיקה באופן הבא: "אי אפשר לבנות מכונה אנרגיה תרמית הפועלת במחזוריות, שהשפעתה היחידה היא הוצאת חום ממקור והמרתו באופן אינטגרלי ל עֲבוֹדָה". בהרחבה, עיקרון זה מוביל אותנו למסקנה כי:
א) תמיד אפשר לבנות מכונות תרמיות שהיעילות שלהן היא 100%.
ב) כל מנוע חום צריך רק מקור חום אחד.
ג) חום ועבודה אינם כמויות הומוגניות.
ד) כל מנוע חום שואב חום ממקור חם ודוחה חלק מאותו חום למקור קר.
ה) רק עם מקור קר, שתמיד נשמר ב-0 מעלות צלזיוס, יהיה אפשר למנוע חום מסוים להמיר חום כולו לעבודה.
פתרון הבעיה:
חלופה D. עיקרון זה מודיע לנו שאי אפשר להוציא את כל החום מהמקור החם ולהעבירו למקור הקר.
הערה
|1| קורס פיזיקה בסיסי: נוזלים, תנודות וגלים, חום (כרך 2).
מאת פמלה רפאלה מלו
מורה לפיזיקה
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/fisica/segunda-lei-da-termodinamica.htm