בתוך הטקסט "ריכוז במול / ליטר או מולאריותראית שהריכוז במול / ליטר מתייחס לכמות החומר במומס (n1, נמדד במולים) עם נפח התמיסה בליטר (V). עם זאת, ישנם כמה מומסים שכאשר הם מונחים במים הם יוצרים יונים.
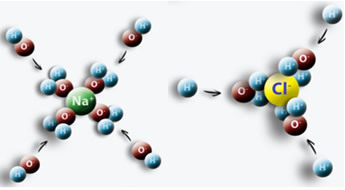
דוגמה לכך היא כאשר אנו מכניסים מלח (NaCl) למים, מתרחשת משיכה בין הקוטב החיובי של המים עם Cl לבין הקוטב השלילי עם Na ויוצר יונים של Na+ וקל-.
חשוב לדעת כיצד לקבוע את הריכוז במול / ליטר של יונים אלה, מכיוון שזה יכול להיות שימושי במצבים רבים. אחד האזורים המשתמשים בכך הוא תרופה, במיוחד בבדיקות דם רפואיות. בדם ובנוזלי הגוף האחרים שלנו יונים מומסים. אם ריכוז היונים הללו בדם שלנו הוא מעל או מתחת לנורמלי, זה יכול לפגוע בתפקוד התקין של גופנו ולהוביל להפרעות ומחלות.
ראה את המקרה של יוני ברזל (Fe2+): אם לאדם חסר יון זה, הוא יכול לפתח אנמיה. לפיכך, כאשר נאמר למישהו הסובל מאנמיה כי עליו לצרוך מזון עשיר בברזל או אפילו תרופה כלשהי המכילה ברזל, זהו למעשה יון הברזל ולא היסוד המתכתי.
מקרה נוסף הוא כאשר יש אובדן של יונים של סידן (Ca2+בעצמות, הגורמות לאוסטאופורוזיס, כפי שמוצג בתמונות עם תמונות מוגדלות של עצמות למטה:

בדוק דוגמאות אחרות ליונים שיש להם פונקציות חיוניות בגופנו ושצריכות להיות בריכוז הנכון:

לכן, בהינתן מידע זה, מתברר כי לדעת באמת לחשב את ריכוז היונים בתמיסות. אך כיצד ניתן לעשות זאת?
ניתן לקבוע את הריכוזים במול / ליטר של היונים הקיימים בתמיסות אם ידועים שני נתונים חיוניים שהם:
- נוסחאות החומרים המומסות במים;
- מולריות הפתרונות שלך.
עם נתונים אלה ביד, כתוב את משוואת הדיסוציאציה או היינון של המומס הנדון ומצא על ידי ניכוי את ריכוז היונים, כ הוא פרופורציונלי למספר השומות של כל יון. משמעות הדבר היא שריכוז היונים הוא פרופורציונלי למקדמיהם בהתאמת יינון או דיסוציאציה.
עיין בדוגמה הבאה כדי להבין טוב יותר כיצד מתבצע חישוב זה:
"קח בחשבון כי הריכוז בכמות החומר של תמיסה מימית נתונה של מגנזיום פוספט (מג3(אָבָק4)2 הוא 0.5 mol / L. מה יהיה הריכוז במול / ליטר של קטיונים מגנזיום (מג2+(פה)) ואניוני פוספט (PO3-4 (aq)) בפתרון זה, בהתחשב בכך שמידת הדיסוציאציה (α) הייתה 100%? "
השלב הראשון בפתרון בעיה זו הוא כתיבת משוואת דיסוציאציה או יינון. אם אתה מתקשה, תוכל להתבסס על המשוואה הגנרית שלמטה:
1 אאיקסבy → x א+ y + y B-איקס
1 mol x mol y mol
לכן, בהתחשב בדוגמה זו שמגנזיום פוספט התנתק לחלוטין, יש לנו את המשוואה הבאה:
1 מ"ג3(אָבָק4)2 (aq) → 3 מ"ג2+(פה) + 2 נ"פ3-4 (aq)
1 mol 3 mol 2 mol
אנו יכולים לראות כי 1 שומה של מג3(אָבָק4)2 נותן 3 mol של Mg2+(פה) ו- 2 mol PO3-4 (aq); לפיכך, מספר השומות של הקטיון יהיה פי 3 ממספר השומות של הפוספט איתן הוכן התמיסה, וזה של האניונים יהיה פי 2.
כיוון שהפתרון הוא 0.5 mol / L של Mg3(אָבָק4)2 (aq) , פירוש הדבר כי 0.5 מול של Mg מומס ב 1 ליטר ממנו3(אָבָק4)2, שהוליד 1.5 mol / L של Mg2+(פה) ו- 1.0 mol / L של PO3-4 (aq):
1 מ"ג3(אָבָק4)2 (aq) → 3 מ"ג2+(פה) + 2 נ"פ3-4 (aq)
1 mol 3 mol 2 mol
0.5 מול x y
1. 0,5 3. 0,5 2. 0,5
0.5 מול / ליטר 1.5 מול / ליטר1.0 mol / L
אבל מה אם מידת הדיסוציאציה או היינון לא הייתה 100%? בואו נגיד שזה היה 70%, איך נצא לגלות את ריכוז mol / L של היונים האלה?
במקרה כזה, פשוט בצע כלל פשוט של שלושה. ראה למטה:
1.5 mol / L של Mg2+(פה) 100 %
x 70%
x = 70. 1,5 → x = 1.05 mol / L של יונים Mg2+(פה)
100
1.5 mol / L של PO3-4 (aq) 100 %
y 70%
y = 70. 1,0 → y = 0.70 mol / L של יוני PO3-4 (aq)
100
מאת ג'ניפר פוגאצה
בוגר כימיה
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/quimica/concentracao-dos-ions-mol-l.htm


