חומצות ובסיסים הם שני סוגים של חומרים מאכלים, אך הם נחשבים הפכים כימיים.
אחד ההבדלים הגדולים ביותר בין חומצות לבסיסים הוא שבסיסים, במגע עם תמיסה מימית, משחררים יונים שליליים, הידרוקסילים (OH-). חומצות, במגע עם מים, משחררות יוני מימן חיוביים (H+).
כל חומר בעל ערך pH בין 0 ל-7 נחשב לחומצי, בעוד שערך pH של 7 עד 14 הוא בסיס. הערך 7 הוא ניטרלי, המתאים למים.
| חומצות | בסיסים | |
|---|---|---|
| הגדרה של Arrhenius | חומצה היא כל תרכובת כימית שבתמיסה מימית משחררת יוני מימן (H+). |
בסיס, או אלקלי, הוא חומר שבתמיסה מימית משחרר הידרוקסילים, יונים שליליים (OH-) |
| הגדרה של ברונסטד-לאורי | חומצה היא חומר התורם פרוטון. | בסיס הוא כל חומר שמקבל פרוטון. |
| הגדרה של לואיס | במהלך קשר כימי, חומצות הן אלו שמקבלות זוגות אלקטרונים. | בקשר כימי, הבסיסים הם אלה שתורמים זוגות אלקטרונים. |
| ערך חומציות | פחות מ-7.0. | יותר מ-7.0. |
| מאפיינים פיזיים | חומצות יכולות להופיע בצורה מוצקה, נוזלית או גזית, תלוי בטמפרטורה. | לרוב מוצק מלבד אמוניה שהיא גז. |
| מִבְנֶה | חומצות הן מולקולריות, כלומר נוצרות על ידי קשרים קוולנטיים שבהם אלקטרונים משותפים. | הבסיסים יכולים להיות יוניים או מולקולריים. |
| נוסחה כימית | לחומצות יש נוסחה כימית עם H בהתחלה, למשל, HCl (חומצה הידרוכלורית). חומצה אצטית (חומץ) היא חריגה, עם CH3COOH. | לבסיסים יש OH בסוף הנוסחה שלהם, למשל NaOH (נתרן הידרוקסיד). |
| מסיסות במים | הם נוטים להיות מסיסים למדי במים. | רוב הבסיסים כמעט בלתי מסיסים. |
| תגובה על מחוון פנולפתלין | זה נשאר חסר צבע. | הפוך את הפתרון לוורוד. |
| מבחן Ph (עם נייר לקמוס) | זה הופך לאדום. | זה הופך לכחול. |
| מוליכות חשמלית | הם מוליכים חשמל רק כשהם מומסים במים. | הם גם מוליכים זרם חשמלי בתמיסה מימית. |
| דוגמאות | חומצה אצטית, חומצה גופרתית. | נתרן הידרוקסיד, אמוניה |
מהן חומצות ובסיסים
חומצות הן תרכובות יוניות שכאשר הן מומסות במים יוצרות יון מימן חיובי (H+). בסיסים, לעומת זאת, הם תרכובות יוניות היוצרות יון הידרוקסיד (OH-) בעל מטען שלילי במים.
הגדרה זו, שנוצרה על ידי המדען השוודי Svante Arrhenius, היא הנפוצה ביותר לסיווג חומצות ובסיסים, עם זאת, יש הגדרות אחרות.
ההגדרה שניתנה על ידי יוהנס נ. ברונסטד ותומס לורי, המכונה הגדרת הפרוטון, אומרים שחומצות הן חומרים שתורמים פרוטון, בעוד שבסיסים הם אלה שמקבלים פרוטון.
בהגדרה שנתן הצפון אמריקאי גילברט ניוטון לואיס, חומצות הן חומרים המקבלים זוגות אלקטרונים בקשר כימי, בעוד שבסיסים מסירים זוגות.
pH של חומצות ובסיסים
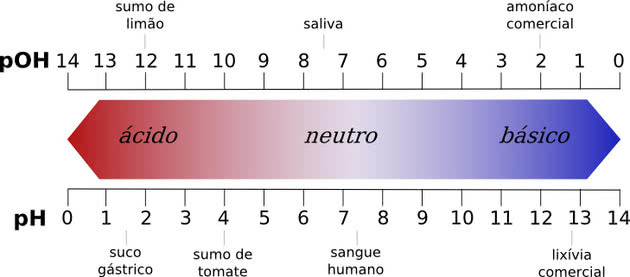
לכל התרכובות הכימיות יש ערך pH, שיכול לנוע בין 0 ל-14, כאשר המספרים מייצגים את ריכוז יוני המימן בתמיסה.
pH ניטרלי הוא ה-pH של מים טהורים, שהוא 7. כל חומר בעל ערך pH בין 0 ל-7 נחשב לחומצי, בעוד שערך pH של 7 עד 14 הוא בסיס.
ככל שהחומצה נמוכה מ-7.0, כך היא חזקה יותר. בבסיסים, ככל שערך ה-pH גבוה יותר, כך הוא יהיה חזק יותר.
מאפיינים של חומצות:
- יש לו טעם מר;
- עלול לשרוף את העור בעת מגע;
- עלול לשתות מתכות ועור;
- הופך נייר לקמוס לאדום;
- במחוון האוניברסלי זה מזוהה על ידי צבעים אדומים או כתומים.
מאפיינים של הבסיסים
- טעם עפיצות;
- כאשר נוגעים, אתה מרגיש משהו צמיג;
- בסיסים רבים מגיבים עם חומצות ומייצרים מלחים;
- בסיסים חזקים יכולים להגיב באלימות עם חומצות;
- הבסיסים הופכים לנייר לקמוס לכחול;
אינדיקטורים של חומצות ובסיסים
מדדי pH, או מחווני חומצה-בסיס, הם חומרים המשמשים כדי לגלות אם תמיסה היא חומצה או בסיס.
זה אפשרי בגלל התכונות הפיזיקליות-כימיות שלו, שיש להן את היכולת לשנות צבע בהתאם ל-pH של החומר הנבדק.
מבין האינדיקטורים המלאכותיים הרבים שבהם נעשה שימוש במעבדה, הידועים ביותר הם פנולפתלין, נייר לקמוס ומחוונים אוניברסליים.
- פנולפטלין נשאר חסר צבע במגע עם חומצה, והופך ורוד במגע עם בסיסים.
- נייר לקמוס הופך לכחול עם בסיסים ואדום עם חומצות.
- המחוון האוניברסלי הוא המדויק ביותר מבין מחווני החומצה-בסיס מכיוון שהוא מציג צבעים שונים בהתאם לכל ערך pH.

יישומים לחומצות ובסיסים בחיי היומיום
חומצות משמשות לעתים קרובות להסרת חלודה ממתכות, כאלקטרוליט בסוללות, לעיבוד מינרלים, לייצור דשנים ובנזין, וכתוספים במזון ו מַשׁקָאוֹת.
הבסיסים משמשים בעיקר בניקוי, כמו חומרי ניקוי לשטיפת כלים וסבון כביסה, חומרי ניקוי לתנורים ומסירי כתמים.