המדען פרידריך קולרוש (1840-1910) היה הראשון שהציע למים טהורים להוביל חשמל, אם כי בקנה מידה קטן. הסיבה לכך היא כי מים מתנהגים בצורה אמפוטרית; כלומר, במקרים מסוימים זה מתנהג כמו חומצה ותורמת פרוטונים (H+); ובאחרים זה מתנהג כמו בסיס, מקבל פרוטונים.
משמעות הדבר היא כי מים מבצעים יינון משלהם, על פי המשוואה הכימית המוצגת להלן:
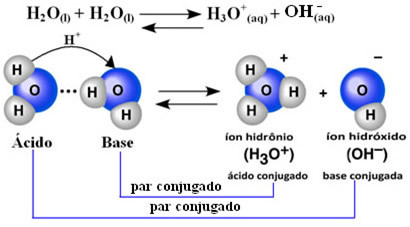
תהליך זה נקרא אוטומציה של מים והיא מתרחשת בקנה מידה קטן מאוד, כלומר מים הם אלקטרוליט חלש מאוד, עם ערכים נמוכים של מידת יינון וקבועת יינון בשיווי משקל (Kç). זו בדיוק הסיבה לכך שלמים יש מוליכות נמוכה כל כך.
כדי לקבל מושג, בטמפרטורת הסביבה של 25 מעלות צלזיוס ניתן לקבוע כי ריכוזי הידרוקסיד ויוני הידרוניום המיוצרים ביינון עצמי של מים טהורים שווים ל -1. 10-7 mol. ל-1. המשמעות היא שמתוך מיליארד מולקולות מים רק שתיים מייננות.
נקרא קבוע האיזון היוני של מים çקבוע לניתוק מים,קבוע אוטומטי פרוטוליזהאוֹ תוצר יוני של מים.קבוע זה מיוצג על ידי קw, כי ה- w מתייחס למילה מים, שפירושו באנגלית water.
חישובו נעשה באותו אופן כמו קבועי שיווי המשקל האחרים, וזכרו שכאמור בטקסט "קבועים של איזון Kc ו- Kp ", במקרה זה, רק המוצרים יופיעו בביטוי מכיוון שלמים במצב נוזלי יש אותה פעילות ל -1. חומרים נוזליים או מוצקים טהורים לא מכניסים לביטוי הקבוע של דיסוציאציה מכיוון שהם אינם משתנים. רק פתרונות מימיים וגזיים ממוקמים. אז יש לנו:
קw = [ח3או+]. [הו-]
קw = (1. 10-7). (1. 10-7)
קw = 10-14
כמו בשאר קבועי שיווי המשקל, בסדרw זה משתנה רק עם שינוי הטמפרטורה. ככל שטמפרטורת המים עולה, גם היינון שלהם עולה, מה שאומר שמינון עצמי של מים הוא תהליך אנדותרמי, כלומר הוא סופג חום.
ניתן לראות זאת בערכי התוצר היוני של מים (Kw) המופיעים בטבלה שלהלן בטמפרטורות שונות:
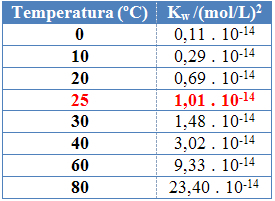
לתוצר היוני של מים תמיד יהיה ערך קבוע בכל טמפרטורה, בין אם במים טהורים ובין אם בתמיסה. גם אם לתמיסה יש ריכוזי יונים H3או+ ואה- שונה, המוצר ביניהם יישאר קבוע.
מאת ג'ניפר פוגאצה
בוגר כימיה
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/quimica/produto-ionico-Agua-kw.htm
