כאשר חומר מחומם, הוא מקבל אנרגיה בצורה כזו שהמולקולות שלו מתסיסות, מתחילות לתפוס נפח גדול יותר, כלומר, הוא עובר התפשטות. ההיפך מתרחש כאשר חומר מתקרר, מכיוון שהוא מאבד אנרגיה והמולקולות שלו נוטות להיות קרובות מאוד זו לזו, מה שגורם להתכווצות בנפח. זה גורם, בדרך כלל, לחומר במצב מוצק לתפוס פחות נפח מאשר כשהוא במצב נוזלי.
בניגוד למה שקורה עם רוב החומרים, למים יש התנהגות חריגה: כאשר הם מחוממים, בין המרווחים של 0 ו-4 מעלות צלזיוס, הם סובלים התכווצות ואז הוא מתחיל להתרחב, כלומר כאשר המים במצב המוצק שלהם, יש להם נפח גדול יותר מאשר במצב נוזלי במרווח זה של טֶמפֶּרָטוּרָה. התנהגות מים לא סדירה זו יכולה להיות מיוצגת באמצעות הגרף הבא:
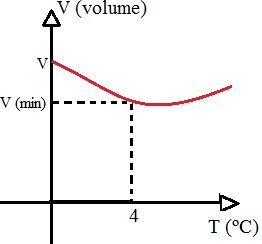
נפח המים יורד בין 0 ל-4 מעלות צלזיוס ואז מתחיל לעלות
אם נפח המים יורד במהלך מרווח זה והמסה שלהם נשמרת קבועה, כתוצאה מכך צְפִיפוּת של מים, שהוא היחס בין מסה לנפח, יהיה מקסימלי כאשר המים בטמפרטורה של 4ºC. תסתכל על הגרפיקה:
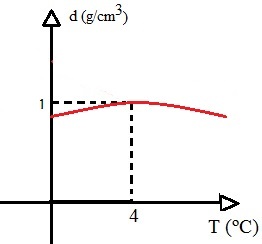
גרף זה מראה שצפיפות המים היא מקסימלית כאשר הטמפרטורה היא 4 מעלות צלזיוס
אבל מה הסיבה להתרחבות החריגה ממים? הסבר זה נמצא בהרכב המולקולרי שלהם. מולקולות מים מחוברות באמצעות קשרים כימיים הנקראים קשרי מימן.
כאשר טמפרטורת המים עולה, מעל 0ºC, קשרי המימן מתחילים להישבר, מה שגורם לקירוב בין המולקולות. השפעה זו מתגברת על התסיסה התרמית המולקולרית, הגורמת למולקולות להתרחק וגורמת להן לתפוס נפח גדול יותר באופן שנפחן מתכווץ.
כאשר הטמפרטורה עולה על 4ºC, מספר קשרי המימן כבר נמוך מאוד. בדרך זו, הריחוק המולקולרי מתחיל לשרוד, ולכן, עלייה בנפחו.
התנהגות מים לא סדירה זו מסבירה כמה תופעות טבע, כולל העובדה שקרח צף על המים, שהוא מה קורה באזורים קרים מאוד, שבהם פני האגמים קפואים בעוד שבתחתית המים נשארים נוזל. מכיוון שלמים יש צפיפות מקסימלית ב-4ºC, הם נשארים בתחתית, מה שיוצר הסעה תרמית, שהיא חילופי חום בגלל ההבדל בצפיפות.
מאת מריאן מנדס
בוגר בפיזיקה
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/fisica/a-agua-seu-comportamento-irregula.htm

