או תרשים שלבים הוא גרף המאפשר לך להגדיר באיזה מצב פיזי חומר נמצא בכל זמן נתון, תוך ידיעת הטמפרטורה והלחץ שלו.
מדידות מעבדה משמשות לבניית דיאגרמת הפאזה של חומר נתון.
התרשים מחולק לשלושה אזורים המייצגים את מצב מוצק, נוזלי ואדי.
הנקודות בקווים התוחמים אזורים אלה מציינות את ערכי הטמפרטורה והלחץ שהחומר יכול להיות בשני מצבים.
דיאגרמת פאזה כוללת את האלמנטים הבאים:
- עקומה של היתוך: מפריד בין האזורים המתאימים למצבים מוצקים ונוזליים.
- עקומה של הִתאַדוּת: מפריד בין האזורים המתאימים לשלבי הנוזל והאדים.
- עקומה של הַאֲצָלָה: מפריד בין האזורים המתאימים לשלבי המוצק והאדים.
- נקודה משולשת: נקודת חיתוך של שלושת העקומות (היתוך, אידוי וסובלימציה). נקודה זו מציינת את ערכי הטמפרטורה והלחץ שהחומר יכול להיות בו זמנית בשלושת המצבים.
- נקודה קריטית: מציין את הטמפרטורה הגבוהה ביותר שהחומר הוא אדי. מאותה נקודה ואילך, לא ניתן עוד להבדיל בין מצבי נוזל לאדים. בטמפרטורות מעל הנקודה הקריטית, החומר הופך לגז.
באיור שלהלן אנו מציגים ייצוג של דיאגרמת פאזה:

קרא עוד ב: שינויים במצב הפיזי.
עקומת התכה
חומרים, באופן כללי, גדלים בנפח כאשר הם עוברים היתוך, ולהפך, ירידה בנפח כשהם מתמצקים. כתוצאה מכך, עלייה בלחץ מובילה לעלייה בנקודת ההיתוך (טמפרטורת ההיתוך).
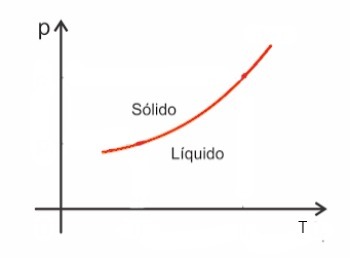
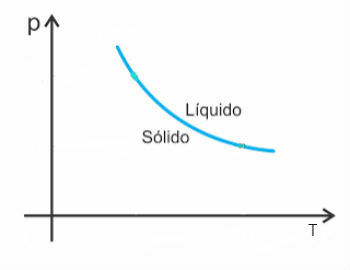
עם זאת, ישנם כמה יוצאים מן הכלל ביניהם מים, אשר בהתכה יורדת בנפחם. במקרה זה, עלייה בלחץ גורמת לירידה בנקודת ההיתוך.
לפיכך, עקומת ההיתוך של חומרים אלה תיראה כך:
דוגמא
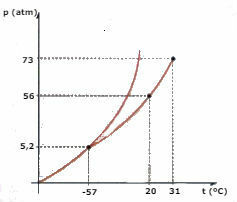
שקול את דיאגרמת שלב ה- CO2 (פחמן דו חמצני) המיוצג להלן ועונה על השאלות:
א) איזה שלב הוא CO2 , כאשר הטמפרטורה שלך היא -60 ° C והלחץ הוא 50 atm?
ב) כמות מסוימת של CO2 נוזל מופעל ללחץ של 56 אטום, והוא מוגבל במיכל. אם מחממים את הנוזל ושומרים על לחץ קבוע, מה ערך הטמפרטורה בו תתרחש אידוי?
ג) מהו טמפרטורת ולחץ הנקודה המשולשת של CO2?
ד) חתיכת קרח יבש (CO2) נתון ללחץ של 2 כספומטים. הוא מחומם, תוך שמירה על לחץ קבוע. ברגע מסוים מתחיל להתרחש שינוי פאזה. מה שמו של השינוי הזה?
פתרון הבעיה:
א) בהתבוננות בתרשים, אנו מסיקים כי ה- CO2 יהיה בשלב האיתן.
ב) אידוי יתרחש כאשר הטמפרטורה מגיעה ל -20 מעלות צלזיוס.
ג) נקודת המשולש מתאימה לצומת שלושת העקומות, במקרה של CO2, כאשר יש לו טמפרטורה של -57 ° C ולחץ של 5.2 atm, שלושת המצבים הפיזיים יכולים להתקיים יחד.
ד) סובלימציה תתרחש
למידע נוסף, קרא גם:
- התמצקות
- נקודת התכה ורתיחה
- אידוי
- הִתְעַבּוּת
תרגילים נפתרו
1) האויב - 2000
גם כיום מקובל מאוד שאנשים משתמשים במיכלי חרס (צנצנות או סירי קרמיקה לא מזוגגים) כדי לחסוך במים בטמפרטורה נמוכה מזו של הסביבה. זה בגלל ש:
א) חימר מבודד מים מהסביבה ושומר אותם תמיד בטמפרטורה נמוכה מזו, כאילו היה קלקר.
ב) לחומר יש הכוח "להקפיא" מים בשל ההרכב הכימי שלהם. בתגובה, מים מאבדים חום.
ג) החימר נקבובי ומאפשר למים לעבור דרכו. חלק ממים אלה מתאדים, לוקח חום מהמורינגה ומשאר המים, שמקוררים לאחר מכן.
ד) החימר נקבובי ומאפשר מים להתיישב בחלקו החיצוני של הכד. המים החיצוניים תמיד נמצאים בטמפרטורה גבוהה יותר מבפנים.
ה) מורינגה הוא סוג של מקרר טבעי, המשחרר חומרים היגרוסקופיים המפחיתים באופן טבעי את טמפרטורת המים.
חלופה ג ': חימר נקבובי ומאפשר מעבר של מים. חלק ממים אלה מתאדים, לוקח חום מהמורינגה ומשאר המים, שמקוררים לאחר מכן.
2) איטה - 2013
שקול את תרשים השלבים ההיפותטי המיוצג באופן סכמטי באיור הבא:

מה מייצגות נקודות A, B, C, D ו- E?
נקודה א ': נקודת סובלימציה
נקודה B: נקודה משולשת
נקודת C: נקודת התכה / התמצקות
נקודה D: נקודת אידוי / עיבוי
נקודה ה ': נקודה קריטית
3) UECE - 2009
כאשר מסתכלים על דיאגרמת שלב ה- PT המוצגת להלן ניתן להסיק, נכון, כי חומר שעבר תהליך סובלימציה עוקב אחר המסלול:

א) X או Y
ב) Y או U
ג) U או V.
ד) T או X
חלופה b: Y או U