ניסויים הם דרך מעשית ללמוד ולבדוק את הידע שלך לגבי המושגים הנלמדים בכימיה.
נצל את הניסויים הכימיים האלה, שניתן לעשות בבית (בהשגחת מבוגר) או לעבוד עליהם בכיתה עם המורה, כדי להשלים את הלימודים שלך.
חוויה 1 - פרום הצבעים
מושגים מעורבים: כרומטוגרפיה והפרדת תערובות
חומרים
- עטים (טושים מסומנים) בצבעים שונים
- כּוֹהֶל
- נייר סינון קפה
- כוס (כוס כדי להקל על ניטור הניסוי)
איך להכין
- השתמש במספריים וחתוך רצועות נייר סינון. עבור כל עט בשימוש, הכינו מלבן.
- כעת, במרחק של כ -2 ס"מ מהבסיס, צייר עיגול בעט הצבע שבחרת וצייר את כל החלק הפנימי.
- הדביקו את קצה הנייר הרחוק ביותר מהשיש הנמשך על גבי תומך. לשם כך תוכלו להשתמש בסרט ולהצמידו לעיפרון.
- הוסף אלכוהול לכוס, לא יותר מדי, מכיוון שהוא צריך לגעת רק בקצה הנייר ליד סימן העט.
- הניחו את הנייר בכוס כך שהוא יהיה אנכי. העיפרון התומך בו צריך לנוח על הקצוות.
- המתן בין 10 ל -15 דקות עד שהאלכוהול יעלה דרך נייר הסינון. לאחר מכן, הסר את הניירות ותן להם להתייבש.
תוֹצָאָה
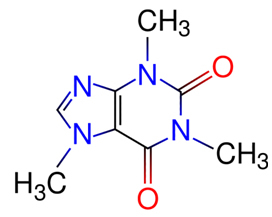
כאשר אלכוהול עובר דרך סימן העט, הוא מתקשר עם רכיבי הצבע ומעביר אותם על הנייר. לפיכך, הפיגמנטים השונים יופרדו על ידי מגע עם אלכוהול.
באמצעות ניסוי זה ניתן לדעת אילו צבעים ערבבו כדי ליצור את צבע העט.
הֶסבֵּר
כרומטוגרפיה היא סוג של תהליך להפרדת תערובות. נייר סינון הוא השלב הנייח ואלכוהול הוא השלב הנייד שגורר את מרכיבי התערובת כשהוא עובר את השלב הנייח. בתהליך זה, ככל שהאינטראקציה עם האלכוהול גדולה יותר, כך הפיגמנט ינוע מהר יותר עם מעבר הממיס.
מרכיבי החומר, מכיוון שיש להם מאפיינים שונים, יתקשרו עם השלב הנייד בדרכים שונות, בהן ניתן להבחין בזמני הגרירה השונים בשלב הנייח.
למידע נוסף על כרומטוגרפיה.
חוויה 2 - שימור אוכל
מושגים מעורבים: תרכובות אורגניות ותגובות כימיות
חומרים
- תפוח, בננה או אגס
- מיץ לימון או תפוז
- לוח ויטמין C
איך להכין
- בחר אחד משלושת הפירות וחתוך אותו לשלושה חלקים שווים.
- היצירה הראשונה תשמש כהשוואה עם האחרים. אז אל תוסיף לזה שום דבר, פשוט השאר אותו חשוף לאוויר.
- לטפטף את תכולת הלימון או התפוז לאחת החלקים. מורחים כך שכל החלק הפנימי של הפרי יתכסה במיץ.
- בחלק האחרון מורחים את ויטמין C, זה יכול להיות לוח כתוש, על כל עיסת הפרי.
- צפו במתרחש והשוו את התוצאות.
תוֹצָאָה
עיסת הפירות שנחשפה לאוויר אמורה להתכהה במהירות. מיץ לימון או תפוז וויטמין C, חומר כימי הנקרא חומצה אסקורבית, אמור להאט את השחמת הפרי.

הֶסבֵּר
כאשר אנו חותכים פרי, תאיו נפגעים ומשחררים אנזימים כגון פוליפנול אוקסידאז, הנמצא ב מגע עם האוויר מחמצן את התרכובות הפנוליות הקיימות במזון וגורם להשחמה אנזימטית.
כדי למנוע את פעולת החמצן משתמשים בחומרים משמרים כגון חומצה אסקורבית מכיוון שהם מחומצנים מעדיפים במקום תרכובות פנוליות. בנוסף לטבליה של ויטמין C, חומצה אסקורבית קיימת גם במקורות טבעיים, כמו הדרים, לימון ותפוז, שהוצעו בניסוי.
למידע נוסף על חִמצוּן.
חוויה 3 - מי קופא מהר יותר?
מושגים מעורבים: תכונות קולגטיביות וקריוסקופיה
חומרים
- שני צינורות (משמשים לחסדי מסיבות)
- קערת זכוכית
- מלח שולחן
- מים מסוננים
- קרח
- מד טמפרטורה
איך להכין
- הוסף את אותה כמות מים מסוננים לשני הצינורות. לדוגמא, 5 מ"ל בכל שפופרת.
- מוסיפים את מלח השולחן לאחד הצינורות ומניחים קלטת זיהוי כדי להבחין איזה מהם מלוח.
- ממלאים את מיכל הזכוכית בקרח כתוש ומוסיפים מעט מלח.
- הנח את שתי הצינורות בו זמנית לתוך הקרח וצפה במה שקורה.
- רשום את טמפרטורת הקפאה לכל סיטואציה.
תוֹצָאָה
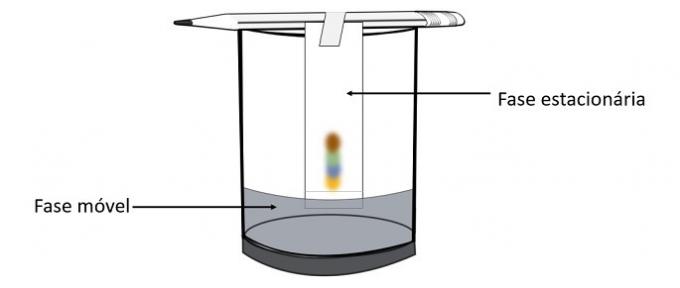
הוספת מומס למים מורידה את טמפרטורת ההקפאה. לכן, מים רגילים נוטים לקפוא הרבה יותר מהר מתמיסת מלח ומים כאשר הם נחשפים לאותם תנאים.
הֶסבֵּר
קריוסקופיה היא מאפיין קולגיטיבי החוקר את השונות בטמפרטורה של ממס כאשר כמוסות מומס שונות מומסות בו.
הורדת טמפרטורת ההקפאה של מים נגרמת על ידי מומס שאינו נדיף ולתופעה זו יש יישומים מעשיים רבים. לכן, ככל שריכוז המומס גדול יותר בתמיסה משפיע על האפקט הקריוסקופי.
אם, למשל, מים קופאים ב 0 מעלות צלזיוס ונוסיף להם מלח, הטמפרטורה לשינוי השלב תהיה שלילית, כלומר נמוכה בהרבה.
זו הסיבה שמי הים לא קופאים במקומות שהטמפרטורה שלהם נמוכה מ- 0 מעלות צלזיוס. מלח מומס במים נוטה להוריד עוד יותר את טמפרטורת ההקפאה. במקומות בהם שלג נהוג גם לזרוק מלח על הכבישים כדי להמיס את הקרח ולהימנע מתאונות.
למידע נוסף על תכונות קולגטיביות.
ניסוי רביעי - פירוק מי חמצן
מושגים מעורבים: תגובה כימית וזרז
חומרים
- חצי תפוח אדמה גולמי וחצי מבושל
- חתיכת כבד גולמי ועוד חתיכה מבושלת
- מי חמצן
- 2 מנות
איך להכין
- בכל מנה מוסיפים אוכל, תפוחי אדמה יחד וכבדים יחד.
- בכל אחד מארבעת החומרים מוסיפים 3 טיפות מי חמצן.
- צפו במתרחש והשוו את התוצאות.
תוֹצָאָה
מי חמצן, תמיסת מי חמצן, כאשר הוא בא במגע עם מזון גולמי, מתחיל להתפשט כמעט באופן מיידי.
ניסוי זה יכול להיעשות גם על ידי הוספת חתיכת מזון למיכל עם מי חמצן כדי להבחין בתגובה.
הֶסבֵּר
ההתפשטות שמציג מי חמצן בבואו במגע עם מזון גולמי מאפיינת את התרחשות של תגובה כימית, שהיא פירוק מי חמצן ושחרור הגז חַמצָן.
הפירוק של מי חמצן מתרחש באמצעות פעולת האנזים הקטלאז, הנמצא באברון הפרוקסיסומים, הקיים בתאי בעלי חיים וצמחים.
חשוב לציין כי הפירוק של מי חמצן מתרחש באופן ספונטני, בנוכחות אור שמש, אך בתגובה איטית מאוד. עם זאת, קטלאז משמש כזרז, מה שמגביר את מהירות התגובה הכימית.
מי חמצן יכול להיות חומר רעיל לתאים. לכן קטלאז מפרק את התרכובת ומייצר מים וחמצן, שני חומרים שאינם פוגעים בגוף.
כאשר אוכל מבושל, מרכיביו עוברים שינויים. שינויים הנגרמים על ידי בישול פוגעים גם בפעולת הקטלאז על ידי דנטורציה של החלבון.
אותה פעולה שאנו רואים במזון היא מה שקורה כאשר אנו שמים מי חמצן על פצע. קטלאז פועל ויש היווצרות בועות, המורכבת משחרור חמצן.
למידע נוסף על תגובה כימית.
הפניות ביבליוגרפיות
סיינטס, וו. ל. עמ '; MOL, G. ש. (קואורדינציות). כימיה אזרחית. 1. עורך סאו פאולו: הדור החדש, 2011. v. 1, 2, 3.
החברה הכימית הברזילאית (אורג ') 2010. כימיה בקרבתך: ניסויים בעלות נמוכה לכיתת K-12. 1. עורך סאו פאולו.