תגובה מנטרלת מתרחשת כאשר חומצה מגיבה עם בסיס ליצירת מים ומלח. החומצה מספקת את יוני H+ והבסיס מספק את יוני ה- OH- להיווצרות מים (H2O):
1 שעה+(פה) + 1 OH-(פה) → H2או(ℓ)
סוג זה של תגובה נקרא "נטרול" מכיוון שה- pH של המדיום מנוטרל; ה- pH של המים הוא 7.0 (ניטרלי).
כדי שתגובות אלו יתרחשו יש צורך לשחרר כמות מסוימת של חום, כחלק מהאנרגיה של ה- היונים משמשים ליצירת הקשרים המביאים למולקולות מים, בעוד שאר האנרגיה משתחררת ל דַי. אנרגיה משוחררת זו נקראת אנטלפיה נטרול (.Hנִטרוּל).

אל תפסיק עכשיו... יש עוד אחרי הפרסום;)
מכיוון שהוא משחרר חום, זה תואם לתגובות אקסותרמיות, שבהן האנטלפיה (האנרגיה הגלובלית של המערכת) תמיד תהיה שלילית, פחות מאפס.
במקרה של תגובה בין חומצות חזקות לבסיסים חזקים, ערך האנטלפיה המנטרל תמיד יהיה שווה ל- - 13.8 קק"ל / מול או - 57.7 קג''ן / מול. זה קורה מכיוון שהבסיסים והחומצות החזקות מתנתקים לחלוטין בתמיסה ולכן הם היחידים התגובה האחראית לביטוי החום תהיה היווצרות מים, כפי שמוצג בשלוש הדוגמאות להלן:
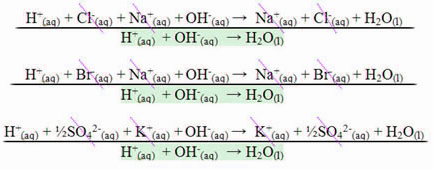
במקרה של תגובות ניטרול הקשורות לחומצות או בסיסים חלשים, ערך האנטלפיה המנטרל יהיה פחות מ -57.7 kJ / mol.
מאת ג'ניפר פוגאצה
בוגר כימיה
האם תרצה להתייחס לטקסט זה בבית ספר או בעבודה אקדמית? תראה:
FOGAÇA, ג'ניפר רושה ורגס. "אנתלפיה של ניטרול"; בית ספר ברזיל. אפשר להשיג ב: https://brasilescola.uol.com.br/quimica/entalpia-neutralizacao.htm. גישה אליו ב -28 ביוני 2021.



