איזומריזם זוהי תופעה טבעית שבה חומרים שונים (מבחינת תכונות כימיות ופיזיקליות) הם בעלי אותה נוסחה מולקולרית בדיוק, כמו בדוגמה הבאה:
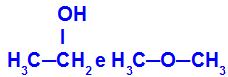
חומרים שונים בעלי אותה נוסחה מולקולרית
לאתנול (משמאל) הנוסחה המולקולרית C2ה6O, המתרחש גם עם metoxxyethane (מימין), ולכן הם איזומרים.
סוגי איזומריזם
→ איזומר שטוח
זהו סוג האיזומריזם החוקר את ההבדלים המבניים בין איזומרים.
ה) כיבוש
זהו סוג האיזומריזם השטוח בו ההבדל בין חומרים מבוסס על ההבדל בין הפונקציות האורגניות אליהן הם שייכים. ראה כמה דוגמאות:
פרופונון ופרופן:
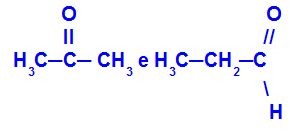
איזומרים השייכים לפונקציות שונות
פרופונון (משמאל) שייך לקבוצת הקטונים, ופרופנאל (ימין) שייך לקבוצת האלדהיד.
ב) כלא
זהו סוג האיזומריזם השטוח בו ההבדל בין חומרים מבוסס על ההבדל בין השרשראות שהם מציגים. ראה דוגמה:
2-מתיל-פרופאן ובוטאן
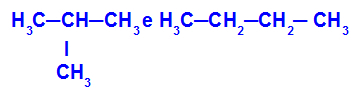
איזומרים שיש להם רשתות עם סיווגים שונים
בדוגמה, אנו יכולים לראות של -2-מתיל-פרופאן (משמאל) יש שרשרת מסועפת, ולבוטן (מצד ימין) יש שרשרת רגילה.
ç) עמדה
זהו סוג האיזומריזם השטוח בו ההבדל בין חומרים מבוסס על הבדל המיקום של רכיב הקיים בשרשראותיהם. ראה דוגמה:
1-כלור-פרופאן ו -2-כלור-פרופאן
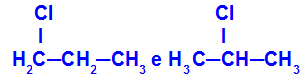
איזומרים שיש להם רכיבים במיקומים שונים בשרשרת
בדוגמה, אנו יכולים לראות כי 1-כלור-פרופן (משמאל) כולל את הכלור על פחמן 1, ו -2-כלור-פרופאן (מצד ימין) את הכלור על פחמן 2.
ד) מטאמריה או פיצוי
הערה: איזומריזם תקף אך ורק למיתרים הטרוגניים.
זהו סוג האיזומריזם השטוח בו ההבדל בין החומרים מבוסס על ההבדל במיקום ההטרו-אטום הקיים בשרשראותיהם. ראה דוגמה:
דוגמא: מתוקסיפרופאן ואתוקסיאתאן
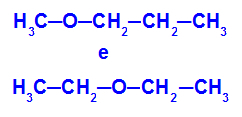
איזומרים שיש להם הטרואטומים במיקומים שונים בשרשרת
בדוגמה, אנו יכולים לראות כי במטרוקסיפרופאן (משמאל), לחמצן יש רדיקל עם פחמן אחד בצד אחד ושלושה פחמנים בצד השני. באתוקסיטאן (מימין), לחמצן יש רדיקל עם שני פחמנים בצד אחד ושני פחמנים בצד השני.
ו)טאוטומריה
זהו מקרה מסוים של איזומריזם של תפקוד מישורי ומתרחש בשלוש פונקציות אורגניות בלבד:
אלדהיד
קטון
אנול
סוג זה של איזומריזם עובד על העובדה שיש איזון כימי בין אנול לאלדהיד ובין אנול לקטון, כלומר, רכיבים אלה הופכים כל הזמן זה לזה. ראה דוגמה:
Prop-2-en-1-ol ופרופונון
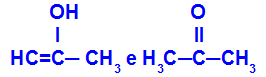
איזומרים השייכים לפונקציות שונות
בדוגמה, אנו יכולים לראות כי Prop-2-en-1-ol (משמאל) שייך לקבוצת האנולים, ופרופנון (מימין) שייך לקבוצת הקטונים, ולכן הם איזומרים של טאוטומריה.
→ איזומריזם בחלל
זהו סוג של איזומריזם המוגדר על ידי הניתוח המרחבי של המולקולה.
א) איזומרים גיאומטריים
אל תפסיק עכשיו... יש עוד אחרי הפרסום;)
זהו סוג של איזומריזם מרחבי המתרחש כאשר לחומר יש מולקולות עם המאפיינים הבאים:
שרשרת סגורה הכוללת שני פחמנים עם שני ליגנדים שונים, כמו בדוגמה שלהלן:

מבנה סגור עם איזומריזם גיאומטרי
שרשרת פתוחה שיש לה קשר כפול בין פחמנים, ובכל אחד מהפחמנים האלה של הקשר הכפול יש שני ליגנדים שונים, כמו בדוגמה שלהלן:
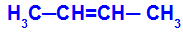
מבנה פתוח עם איזומריות גיאומטרית
איזומריזם גיאומטרי מחולק לשתי קבוצות:
1או קְבוּצָה: סיס-טרנס
זה קורה כאשר שני הליגנדים של פחמן אחד שווים לחלוטין לשני הליגנדים של הפחמן השני, בין אם במבנה הפתוח ובין אם במבנה הסגור.
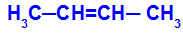
שרשרת של חומר שיש בו איזומריזם cis-trans
האיזומר ייקרא cis כאשר אותם ליגנדים נמצאים באותו מישור.

דוגמה לאיזומר cis
האיזומר ייקרא טרנס כאשר הליגנדים השונים נמצאים באותו מישור.

דוגמה לאיזומר טרנס
2או קְבוּצָה: E-Z
זה קורה כאשר שני הליגנדים של פחמן אחד שונים ביחס לשני הליגנדים של הפחמן השני, במבנה הפתוח או במבנה הסגור.

שרשרת של חומר שיש בו איזומריזם E-Z
האיזומר ייקרא E כאשר הליגנדים עם המספר האטומי הגבוה ביותר נמצאים במישורים מנוגדים. בדוגמה שלהלן, לפחמן משמאל יש את ה- Br עם המספר האטומי הגבוה ביותר (35), ובשני יש חמצן (8).
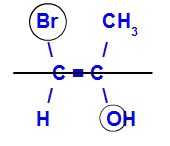
דוגמה ל- E-isomer
האיזומר ייקרא Z כאשר הליגנדים עם המספר האטומי הגבוה ביותר נמצאים באותו מישור. בדוגמה שלהלן, לפחמן משמאל יש את ה- Br עם המספר האטומי הגבוה ביותר (35), ובשני יש חמצן (8).

דוגמה ל- Z-isomer
ב) איזומר אופטי
זהו סוג של איזומריזם מרחבי המתרחש רק אם לחומר יש מולקולות פחמן כיראלי (זה שיש בו ארבעה ליגנדים שונים) במבנים שלהם. למולקולה עם פחמן כיראלי יכולת לקטב ולהסיט את האור כדלקמן:
מימין (איזומר ימני)
משמאל (איזומר levorotatory)
תמיד יש לתרכובת עם פעילות אופטית איזומרים פעילים (נקראים אנטיפודים אופטיים) ואיזומרים לא פעילים (תערובת בין שני איזומרים פעילים, תערובת הנקראת גזעית).
אנו יכולים להשתמש בנוסחה הבאה כדי לקבוע את מספר האיזומרים הפעילים (IOA) והלא פעילים (IOI) של תרכובת שיש לה פחמן כיראלי:
IOA = 2לא
IOI = 2לא
2
להלן דוגמה לתרכובת שיש בה איזומריות גיאומטרית:
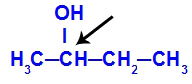
פחמן כיראלי שמופיע בבוטן -2-אול
המבנה של בוטן -2-אול מכיל את הליגנדים הבאים:
מתיל (CH3)
אתיל (CH3-CH2)
מימן (H)
הידרוקסיל (OH)
מכיוון שיש בו רק פחמן כיראלי אחד, יש בבוטן -2-אול:
איזומרים פעילים:
IOA = 21
IOA = 2
איזומרים לא פעילים:
IOI = 21
2
IOI = 2
2
IOI = 1
על ידי. דיוגו לופס דיאס
האם תרצה להתייחס לטקסט זה בבית ספר או בעבודה אקדמית? תראה:
DAYS, דיוגו לופס. "מה זה איזומריזם?"; בית ספר ברזיל. אפשר להשיג ב: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-isomeria.htm. גישה אליו ב -27 ביוני 2021.