שקול את התגובה ההפיכה הגנרית להלן, כאשר האותיות הקטנות תואמות את מקדמי התגובה המאוזנים והאותיות הקטנות הן המגיבים והתוצרים כולם גזיים:

בהתחשב בכל אחד מכיווני התגובה בנפרד, שיעורי ההתפתחות שלהם (Td) ניתנים על ידי:
* תגובה ישירה: aA + bB → cC + dD
את כלישיר = Kישיר. [ה]ה. [B]ב
* תגובה הפוכה: cC + dD → aA + bB
את כלהפוך = Kלַהֲפוֹך. [Ç]ç. [D]ד
קבוע שיווי המשקל הכימי מבחינת ריכוז בכמות החומר (Kç) ומבחינת לחץ חלקי (Kפ) יינתן על ידי חלוקת Kישיר מאת קלַהֲפוֹך.
אז יש לנו:
קישיר. [ה]ה. [B]ב = 1 → קישיר__ = __[Ç]ç. [D]ד___
קלַהֲפוֹך. [Ç]ç. [D]ד קלַהֲפוֹך [ה]ה. [B]ב
להיות, קç =_Kישיר_
קלַהֲפוֹך
אז יש לנו:
קç =__[Ç]ç. [D]ד___ או Kפ =__(Praça)ç. (pD)ד___ |
כאשר p הוא הלחץ החלקי של כל חומר בשיווי משקל.
באופן זה, כל ריכוז מועלה למעריך המקביל למקדם החומר המתאים בתגובה, ו- Kç אין יחידה *.
בנוסף, היבט חשוב מאוד שיש להדגיש הוא שבביטוי זהאין לייצג רכיבים מוצקים ולא נוזלים טהורים., שכן רק עניינים שיכולים לסבול משתנות משתתפים בביטוי זה. הריכוז בכמות החומר של חומר במצב מוצק הוא קבוע ולכן הוא כבר נכלל בערך K עצמו.
ç. כנ"ל לגבי נוזלים טהורים כמו מים. בקצרה, רק חומרים במצב גזי ובתמיסה מימית משתתפים בביטוי.אל תפסיק עכשיו... יש עוד אחרי הפרסום;)
שימו לב לדוגמאות הבאות:
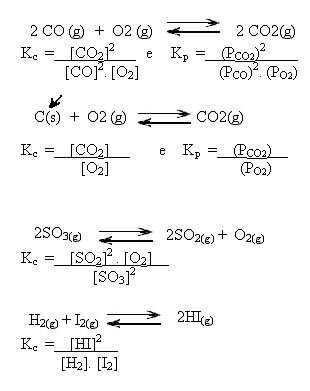
ערכי Kç יכול להראות לנו אם ריכוז המגיבים והמוצרים זהה או שהאחד גדול מהשני:
- אם קç או Kפ שווה לאחד (Kç = 1), המשמעות היא שריכוז המגיבים והמוצרים שווה;
- אם הערך של קç או Kפ להיות גבוה, פירוש הדבר שהמוצרים נמצאים בריכוז גדול יותר, מכיוון שבביטוי של Kç המוצרים נמצאים במניין;
- אם הערך של קç או Kפ נמוך, פירוש הדבר שהריאגנטים נמצאים בריכוז גבוה יותר, מכיוון שבביטוי של Kç ריאגנטים נמצאים במכנה.
* קç ו- Kפ הם מספרים חסרי ממד, כלומר מספרים טהורים, ללא יחידה שקשורה לכל גודל או קשר בין גודל.
מאת ג'ניפר פוגאצה
בוגר כימיה
האם תרצה להתייחס לטקסט זה בבית ספר או בעבודה אקדמית? תראה:
FOGAÇA, ג'ניפר רושה ורגס. "קבועי שיווי המשקל Kc ו- Kp"; בית ספר ברזיל. אפשר להשיג ב: https://brasilescola.uol.com.br/quimica/constantes-equilibrio-kc-kp.htm. גישה אליו ב -28 ביוני 2021.