חוק הס נוצר על ידי הכימאי השוויצרי ז'רמן ה '. הס (1802-1850), שנחשב לאחד ממייסדי התרמו-כימיה. החוק שלו אמר:

כלומר, ΔH תלוי רק בערכי האנטלפיה של ריאגנטים ומוצרים, כמו בביטוי:
| ΔH = ΔHריאגנטים + ΔHמוצרים |
לדוגמא, שקול את התגובה היכן שמול 1 מים (H2O) הופך למים במצב גזי. תגובה זו מבוצעת פעמיים; עם זאת נבחרו מסלולים שונים:
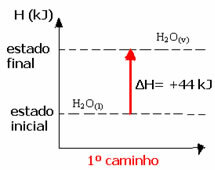
(1) זה בוצע בשלב אחד:
ה2או(1) → H2או(v) ΔH = +44 kJ
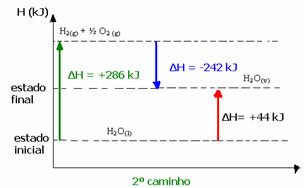
(2) זה בוצע בשני שלבים:
שלב ראשון: ח2או(1) → H2 (גרם) + ½ ה2 (גרם) ΔH = +286 kJ
שלב שני: ח2 (גרם) + ½ ה2 (גרם) → H2או(v) ΔH = -242 kJ
ה2או(1) → H2או(v) ΔH = +44 kJ
אל תפסיק עכשיו... יש עוד אחרי הפרסום;)
שים לב שלא משנה אם בוצעו צעד אחד או שניים, שינוי האנטלפיה (ΔH) הוא תמיד 44 kJ. הסיבה לכך היא ש- ΔH הוא הסכום האלגברי של ערכי valoresH של השלבים המרכיבים את התהליך, כלומר של תהליכי הביניים:
| ΔH = ΔH1 + ΔH2 + ΔH3 + ... |
לדוגמה, במקרה השני, סך כל ה- ΔH של התגובה היה סכום ה- ΔH של הצעד הראשון (ΔH = +286 kJ) עם זה של השני (ΔH = -242 kJ). לפיכך, השגנו את אותו ערך תגובה בשלב אחד:
ΔH = (+286 + (-242)) kJ
ΔH = (+286 -242) kJ
ΔH = +44 kJ
לכן, אנו מעוניינים רק בערכים הראשוניים והסופיים. במקרה זה, המצב ההתחלתי תואם ל- H2או(1) והסוף לה '2או(v).
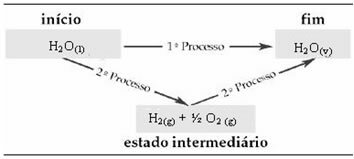
חוק זה הפך להיות חשוב מאוד בתרוכימיה, מכיוון שלא ניתן לקבוע באופן ניסיוני את ΔH שלהם בתגובות כימיות מסוימות. עם זאת, על פי חוק הס ניתן לחשב את האנטלפיה של תגובה מסוג זה מתוך האנטלפיות של תגובות אחרות (תגובות ביניים).
מאת ג'ניפר פוגאצה
בוגר כימיה
צוות בית הספר בברזיל
האם תרצה להתייחס לטקסט זה בבית ספר או בעבודה אקדמית? תראה:
FOGAÇA, ג'ניפר רושה ורגס. "חוק הס"; בית ספר ברזיל. אפשר להשיג ב: https://brasilescola.uol.com.br/quimica/lei-hess.htm. גישה אליו ב -28 ביוני 2021.