קשירה קוולנטית מתרחשת כאשר שני אטומים חולקים זוגות אלקטרונים במטרה לרכוש את תצורת האלקטרונים של גז אצילי (עם 8 אלקטרונים במעטפת הערכיות או עם 2, במקרה של אלה עם מעטפת K בלבד), על פי הכלל של שְׁמִינִיָה.
עם זאת, ישנם מקרים מיוחדים של קשרים קוולנטיים בהם צמד האלקטרונים המשותף מגיע רק מאחד האטומים שכבר יציבים. בעבר נקרא סוג זה של קשר קוולנטי דטיב, היום זה נקרא בדרך כלל יותר לְתַאֵם.
ראה כמה דוגמאות כדי להבין כיצד זה קורה:
- CO (פחמן חד חמצני):
בפחמן יש 4 אלקטרונים בקליפת הערכיות שלו. לכן, על פי כלל האוקטט, כדי להיות יציב, הוא צריך לקבל 4 אלקטרונים נוספים, בסך הכל 8. לעומת זאת, לחמצן יש 6 אלקטרונים במעטפת הערכיות והוא צריך לקבל 2 אלקטרונים כדי לשמור על תצורת ניאון הגז האצילי.
אז ראשית, פחמן וחמצן חולקים שני זוגות אלקטרונים כך שהחמצן יציב:
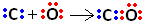
עם זאת, פחמן נשאר לא יציב מכיוון שיש לו עדיין 6 אלקטרונים וצריך 2. לכן, חמצן, שכבר יציב, חולק את אחד מזוגות האלקטרונים שלו עם פחמן, כלומר, הוא יוצר איתו קשר דטיבי, מה שהופך אותו ליציב:

שים לב כי הקשר הקוולנטי הקואורדינט יכול להיות מיוצג על ידי מקף, בדיוק כמו הקשר הקוולנטי הנפוץ.
- רק2 (דו תחמוצת גופרית):
בכל אטום גופרית וחמצן יש 6 אלקטרונים בקליפות הערכיות שלהם, ולכן הם צריכים לקבל 2 אלקטרונים כל אחד. בתחילה, גופרית יוצרת שני קשרים קוולנטיים נפוצים, חולקים שני זוגות אלקטרונים עם אחד מאטומי החמצן, שניהם נשארים יציבים עם 8 אלקטרונים.
אל תפסיק עכשיו... יש עוד אחרי הפרסום;)
אבל אטום החמצן האחר אינו יציב, ולכן הגופרית חולקת איתו זוג אלקטרונים באמצעות קשר קוולנטי מתואם או דטיבי:
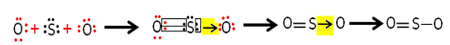
שימו לב שבמקרה זה יש לנו שלושה אטומים במולקולה, כך שיכולה להיות נדידה של הקשר מאטום אחד למשנהו. ניתן לייצג את מולקולת הגופרית הדו-חמצנית כך: O ─ S ═ O.
אנו קוראים לתופעת מליטה זו תְהוּדָה. ראה שלוש דוגמאות נוספות בטבלה למטה:
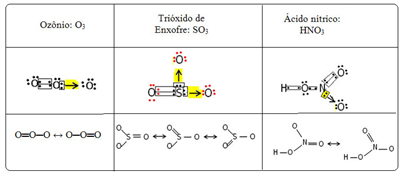
מבנים אפשריים נקראים מבני תהודה אוֹ צורות קנוניות.
סוג זה של קשר קורה גם בהיווצרות יונים, כמו במקרה של יונים הידרוניום (H3או+) ואמוניום (NH4+).
ראשית, הקטיון H+ הוא נוצר כאשר מימן מאבד את האלקטרון היחיד שלו, ומשאיר אותו עם מטען חיובי. כך שיהיה צורך לקבל שני אלקטרונים כדי להיות יציבים. זה קורה דרך קשר דטיבי עם מים (במקרה של יון הידרוניום) ועם אמוניה (במקרה של יון האמוניום). שעון:

מאת ג'ניפר פוגאצה
בוגר כימיה
האם תרצה להתייחס לטקסט זה בבית ספר או בעבודה אקדמית? תראה:
FOGAÇA, ג'ניפר רושה ורגס. "מליטה קוולנטית מקורית או מתואמת"; בית ספר ברזיל. אפשר להשיג ב: https://brasilescola.uol.com.br/quimica/ligacao-covalente-dativa-ou-coordenada.htm. גישה אליו ב -28 ביוני 2021.


