שכבת הערכיות זוהי השכבה (או הרמה) החיצונית ביותר (הרחוקה ביותר מהגרעין) של אטום, כלומר זו הרחוקה ביותר מהגרעין. לכן, יש לו מה שנקרא האלקטרונים החיצוניים ביותר או אלקטרוני הערכיות.
מספר הרמות שיכולות להיות לאטום משתנה בין 1 ל -7, עם רמת המשנה הבאה (בצהוב):
רמה K (שכבה 1): רמת משנה ס
רמה L (שכבה 2): גבהות משנה ס ו פ
רמה M (שכבה שלישית): רמת משנה ס, פ ו ד
רמה N (שכבה רביעית): גובה משנה ס, פ, ד ו f
רמה O (שכבה 5): תת גבהים ס, פ, ד ו f
רמה P (נדבך 6): תת גובה ס, פ ו ד
רמה Q (שכבה ראשונה): תת גבהים ס ו פ
בכל אחת מתתי המשנה יש מספר שונה של אלקטרונים. תראה:
רמת משנה s מחזיקה מקסימום 2 אלקטרונים;
רמת משנה p מחזיקה מקסימום 6 אלקטרונים;
רמת משנה d מחזיקה מקסימום 10 אלקטרונים;
רמת משנה f מחזיקה מקסימום 14 אלקטרונים.
לפיכך, אם מעטפת הערכיות של אטום מסוים היא M, המספר המרבי של אלקטרונים שיכולים להיות נוכחים בו הם 18 (2 אלקטרונים מרמת המשנה + 6 אלקטרונים מרמת המשנה p + 10 אלקטרונים מה- רמת משנה ד).
כדי לקבוע את מעטפת הערכיות של אטום וכמה אלקטרונים יש לו, ישנן שתי דרכים, כלומר:
→ קביעת מעטפת הערכיות ומספר האלקטרונים שלה מהפצה אלקטרונית
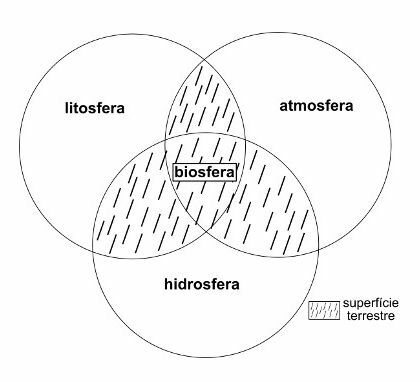
הפצות אלקטרוניות מתבצעות תמיד דרך תרשים לינוס פאולינגמיוצג למטה:

ייצוג תרשים לינוס פאולינג
רגיל מספר אטומי (המציין את מספר האלקטרונים באטום), אנו מבצעים את ההפצה האלקטרונית. לדוגמא, אטום של מספר אטומי 50:

התפלגות אלקטרונית של האטום של מספר האטום השווה ל 50
בניתוח ההתפלגות שלעיל, יש לנו שהרמה הרחוקה ביותר מהגרעין היא הרמה החמישית (N), בה יש לנו נוכחות של 4 אלקטרונים (שניים ברמה התחתונה ו- 2 ברמת המשנה p).
→ קביעת מעטפת הערכיות ומספר האלקטרונים שלה מהטבלה המחזורית
הטבלה מסודרת בתקופות (עמודות אופקיות), המציינות את מספר רמות האטום, וקבוצות או משפחות (עמודות אנכיות). התקופה משמשת לקביעת ה- שכבת הערכיות, והמשפחות משמשות לקביעת מספר האלקטרונים.
א) הכרת תקופת היסוד הכימי
הטבלה המחזורית מציגה בסך הכל שבע תקופות, אשר מספרן קשור למספר הרמות הקיימות בתרשים לינוס פאולינג. אז אם אנו יודעים את התקופה שבה יסוד כימי הוא נמצא בטבלה באופן אוטומטי, אנו יודעים כמה רמות יש לאטומים שלך, שכבת הערכיות היא הרמה הרחוקה ביותר מהגרעין.
דוגמה ראשונה: יסוד כימי אֶשׁלָגָן
אשלגן ממוקם בתקופה הרביעית של הטבלה המחזורית, ולכן האטום שלו כולל ארבעה רמות, כאשר הרמה הרביעית היא שכבת הערכיות, המאושרת באמצעות תפוצתה מכשירי חשמל.
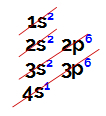
הפצה אלקטרונית של יסוד אשלגן
דוגמה שנייה: יסוד כימי פלוּאוֹר
פלואור ממוקם בתקופה השנייה של הטבלה המחזורית, כך שלאטום שלו יש שניים רמות, כאשר הרמה השנייה היא שכבת הערכיות, המאושרת באמצעות תפוצתה מכשירי חשמל.

הפצה אלקטרונית של יסוד הפלואור
דוגמה שלישית: יסוד כימי אינדיום
ההודי ממוקם בתקופה החמישית של הטבלה המחזורית, כך שיש לאטום שלו חמש רמות, כאשר הרמה החמישית היא שכבת הערכיות, המאושרת באמצעות תפוצתה מכשירי חשמל.

הפצה אלקטרונית של יסוד האינדיום
ב) הכרת המשפחה או הקבוצה של היסוד הכימי
מתוך הכרת המשפחה או הקבוצה בה נמצא היסוד, אנו יודעים גם את מספר האלקטרונים הקיימים בקליפת הערכיות של אותו אלמנט.
אלמנטים ממשפחה א
האלמנטים של המשפחות A ממוקמים בעמודות 1, 2, 13 עד 18 בטבלה המחזורית. כל אחד מהעמודות הללו מקבל מספר (1 עד 8, ספרה רומאית), המציין בדיוק את מספר האלקטרונים במעטפת הערכיות של היסודות הללו:
טור 1 - משפחת IA = לכולם יש אלקטרון אחד במעטפת הערכיות;
טור 2 - משפחה IIA = לכולם 2 אלקטרונים במעטפת הערכיות;
טור 3 - משפחה IIIA = לכולם 3 אלקטרונים במעטפת הערכיות;
טור 4 - משפחת IVA = לכולם 4 אלקטרונים במעטפת הערכיות;
טור 5 - משפחת VA = לכולם 5 אלקטרונים במעטפת הערכיות;
טור 6 - משפחת VIA = לכולם 6 אלקטרונים במעטפת הערכיות;
טור 7 - משפחה VIIA = לכולם 7 אלקטרונים במעטפת הערכיות;
טור 8 - משפחה VIIIA = לכולם 8 אלקטרונים במעטפת הערכיות.
ראה כמה דוגמאות לקביעת מספר אלקטרוני הערכיות של כמה אלמנטים ממשפחה A:
דוגמה 1: יסוד כימי בריום
הבריום ממוקם במשפחת IIA, ולכן יש לו שני אלקטרונים במעטפת הערכיות, דבר המאושר על ידי תפוצתו האלקטרונית:

הפצה אלקטרונית של יסוד הבריום
דוגמה 2: יסוד כימי אנטימון
אנטימון נמצא במשפחת VA, ולכן יש לו חמישה אלקטרונים במעטפת הערכיות, דבר המאושר על ידי תפוצתו האלקטרונית:

הפצה אלקטרונית של אלמנט האנטימון
דוגמה 3: יסוד כימי קסנון
קסנון נמצא במשפחת VIIIA, ולכן יש לו שמונה אלקטרונים במעטפת הערכיות, דבר המאושר על ידי הפצתו האלקטרונית.

הפצה אלקטרונית של אלמנט הזנון
הערה: היסוד הכימי היחיד השייך למשפחה שאינו תואם את הכלל המוצע הוא הליום. הוא שייך למשפחת VIIIA, אך יש לו רק שני אלקטרונים במעטפת הערכיות. הסיבה לכך היא שמספרו האטומי הוא 2, ולכן אי אפשר שיהיו לו 8 אלקטרונים בקליפת הערכיות כמו שאר האלמנטים במשפחה.
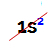
הפצה אלקטרונית של אטום הליום
אלמנטים משפחתיים ב '
האלמנטים של משפחות B ממוקמים בעמודות 3 עד 12 בטבלה המחזורית. כמו גם משפחות A, ישנן גם שמונה משפחות B, המיוצגות על ידי ספרות רומיות. בניגוד למשפחות A, מספר משפחת B אינו קובע את מספר האלקטרונים במעטפת הערכיות.
מספר האלקטרונים במעטפת הערכיות של אלמנט ממשפחת B שווה תמיד ל -2, ללא קשר למספר האטומי ולמיקום בטבלה. ההפצות האלקטרוניות של קליפורניה (98Cf) והאסיוס (108hs) להוכיח זאת:
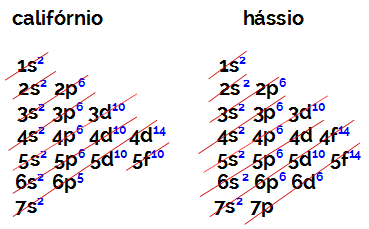
להפצה האלקטרונית של קליפורניה יש רמת המשנה האנרגטית ביותר ב- 5f10, ו- o של חסיוס הוא 6d6. בשני המקרים, רמת המשנה הרחוקה ביותר מהגרעין היא הרמה השביעית, ולשתיהן שני אלקטרונים מבוזרים.
על ידי. דיוגו לופס דיאס
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-camada-valencia.htm