ה גיאומטריה מולקולריתכלומר סידור האטומים של מולקולה יכול להיקבע על ידי כלל הכימאי גילספי, בו הוא מפרט את מספר האטומים המחוברים לאטום מרכזי ואת מספר העננים מכשירי חשמל.
ידע על הגיאומטריה של מולקולה חשוב ביותר מכיוון שהוא עוזר לנו לקבוע את הקוטביות, וכתוצאה מכך, את המסיסות (על פי הכלל של התמוססות דומה דוֹמֶה).
עם השיחה גיאומטריה טטראדרלית, אינו שונה. עיין בקריטריונים לקביעתו על פי כללי גילספי:
מולקולות פנטטומיות (חמישה אטומים);
היעדר עננים אלקטרוניים באטום המרכזי;
מולקולות מרוכבות או אניונים מורכבים.
כמה דוגמאות למולקולות שהגיאומטריה שלהן היא טטרהדרלית הם:
CH4

נוסחת מבנה CH4
בפחמן ארבעה אלקטרונים בקליפת הערכיות שלו וכל האלקטרונים הללו נקשרים עם מימנים. לכן לפחמן אין ענן אלקטרוני (זוג אלקטרונים נוסף).
רק4-2
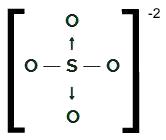
נוסחה מבנית של מערכת ההפעלה4-2
הגופרית, שיש בה שישה אלקטרונים בקליפת הערכיות, יוצרת שני קשרים בודדים עם שני אטומי חמצן ושניים קשרים קוולנטיים דטיביים עם שני החמצנים האחרים. בקשרים בודדים הוא משתמש בשניים מהאלקטרונים שלו ובכל נתיב הוא משתמש בשניים נוספים (בסך הכל ארבעה אלקטרונים המעורבים בתאריכים), ובסך הכל שישה אלקטרונים. ככזה, לא נשאר לו ענן.
NH4+

נוסחת מבנה NH4+
חנקן, בעל חמישה אלקטרונים בקליפת הערכיות, יוצר שלושה קשרים בודדים עם אטומי המימן וקשר דטיבי עם המימן האחר. בקשרים בודדים הוא משתמש בשלושה מהאלקטרונים שלו, ובנתיב זה הוא משתמש בשניים נוספים, הכוללים חמישה אלקטרונים. ככזה, לא נשאר לו ענן.
CH3קל
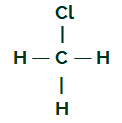
נוסחת מבנה CH3קל
אל תפסיק עכשיו... יש עוד אחרי הפרסום;)
בפחמן ארבעה אלקטרונים בקליפת הערכיות שלו וכל האלקטרונים הללו נקשרים עם המימנים ואטום הכלור. מסיבה זו אין לפחמן ענן אלקטרוני.
→ קוטביות מולקולה
בידיעה שלמולקולה נתונה יש גיאומטריה טטראדרלית, אנו יכולים לקבוע את הקוטביות שלה צורה פשוטה ביותר, שכן המולקולה תפוסה בארבעת הקטבים שלה (ארבעה ליגנדים באטום מֶרכָּזִי). לשם כך, מספיק לדעת את מאפייני הקלסרים ולשקול את אחד הכללים הבאים:
אם מספר העננים שווה למספר הליגנדים השווים = מולקולה לא קוטבית;
אם מספר העננים שונה ממספר הליגנדים השווים = מולקולה קוטבית.
בשתי המולקולות הבאות, שהגיאומטריה שלהן טטרהדרלית, נוכל להחיל את הכללים שלמעלה ולציין את הקוטביות שלהן:
מולקולת מתאן
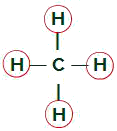
ליגנדים שווים במולקולת המתאן
במולקולת המתאן יש ארבעה ענני אלקטרונים (ארבעה קשרים בודדים) וגם ארבעה אטומי מימן המחוברים לאטום המרכזי. לכן, יש לנוארבעעננים וארבעה קלסרים שווים, בקרוב, ה מולקולה אינה קוטבית.
תַצְפִּית: אם מולקולת החומר היא להתנצל, הוא מתמוסס היטב לחומר אחר שמולקולותיו גם כן לא קוטבי.
מולקולת כלורומטן

ליגנדים שווים במולקולת הכלורומטן
במולקולת הכלורומטן יש ארבעה ענני אלקטרונים (ארבעה קשרים בודדים) ושלושה אטומי מימן ואטום כלור אחד המחובר לאטום המרכזי. לכן, יש לנוארבעעננים ושלושה ליגנדים שווים (שלושה מימנים); בקרוב, ה מולקולה היא קוטבית.
תַצְפִּית: אם מולקולת החומר היא קוֹטבִי, הוא מתמוסס היטב לחומר אחר שמולקולותיו גם כן קוֹטבִי.
על ידי. דיוגו לופס דיאס
האם תרצה להתייחס לטקסט זה בבית ספר או בעבודה אקדמית? תראה:
DAYS, דיוגו לופס. "גיאומטריה טטרהדרלית"; בית ספר ברזיל. אפשר להשיג ב: https://brasilescola.uol.com.br/quimica/geometria-tetraedrica.htm. גישה אליו ב -28 ביוני 2021.