Poiché ci sono eccezioni alla regola dell'ottetto, come facciamo a conoscere la corretta disposizione tra gli atomi nella formazione di una molecola?
Questo può essere fatto calcolando il carico formale di ciascuna struttura. La carica formale più vicina allo zero sarà quella con la maggiore probabilità di esistenza effettiva. Nota che è "più vicino allo zero", quindi non deve essere zero.
La formula della carica formale (Cper) é:
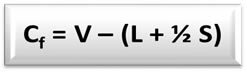
V = numero di elettroni di valenza dell'atomo libero;
L = numero di elettroni presenti nelle coppie isolate (non leganti) dell'atomo nella struttura;
S = numero di elettroni condivisi dall'atomo nella struttura.
Per capire come ciò accade, immagina di voler sapere qual è la struttura elettronica di Lewis per la molecola di SO.2. Abbiamo due possibili disposizioni tra gli atomi:
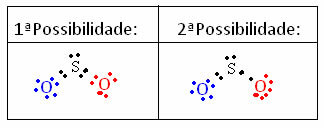
Viene calcolata la carica formale di tutti gli atomi che partecipano alle strutture. Guarda:
1° Possibilità:
Zolfo (S): Ossigeno (O) Ossigeno (O)
Çf(S) = 6 – (2 + ½ 8) Çf(S) = 6 – (4 + ½ 4) Çf(S) = 6 – (4 + ½ 4)
Çf(S) =0 Çf(S) =0 Çf(S) =0
Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
2° Possibilità:
Zolfo (S): Ossigeno (O) Ossigeno (O)
Çf(S) = 6 – (2 + ½ 6) Çf(S) = 6 – (6 + ½ 2) Çf(S) = 6 – (4 + ½ 4)
Çf(S) = +1Çf(S) = -1 Çf(S) =0
Sulla base dei risultati ottenuti, possiamo notare che la 1a struttura è quella con la più alta probabilità di esistenza reale. Quindi, sappiamo che non segue la regola dell'ottetto, ma che lo zolfo ha espanso il suo guscio di valenza, rimanendo stabile con 10 elettroni.
Questa regola si applica anche alla ricerca della corretta disposizione degli ioni.
di Jennifer Fogaça
Laureato in Chimica
Vorresti fare riferimento a questo testo in un lavoro scolastico o accademico? Guarda:
FOGAÇA, Jennifer Rocha Vargas. "Calcolo del carico formale"; Brasile Scuola. Disponibile in: https://brasilescola.uol.com.br/quimica/calculo-carga-formal.htm. Consultato il 28 giugno 2021.