è chiamato fascio ionico la dimensione di uno ione. Lo studio di questa proprietà dipende dalla conoscenza del raggio atomico e degli ioni.
Raggio atomico: è una misura della dimensione di un atomo neutro (distanza teorica dal nucleo all'ultima elettrosfera).
ioni: atomi che perdono (cationi) o acquistano elettroni (anioni).
Protoni all'interno del nucleo di a atomo esercitare una forza attrattiva sugli elettroni (particelle negative) presenti nelle elettrosfere. Maggiore è il numero di protoni, maggiore è questa attrazione e viceversa. Quando il numero di elettroni in un atomo viene modificato da una perdita o guadagno di queste particelle, l'attrazione tra protoni ed elettroni viene modificata come segue:
Nel caso di un catione:
Il numero di elettroni nelle elettrosfere diventa inferiore al numero di protoni all'interno del nucleo, il che fa aumentare la forza di attrazione del nucleo, avvicinandogli gli elettroni. elettrosfere. Il risultato è una diminuzione del raggio dell'atomo. Quindi, il raggio di un catione sarà sempre più piccolo del raggio del suo atomo neutro.
Raggio dell'atomo neutro > Raggio del catione
Nel caso di un anione:
Il numero di elettroni nelle elettrosfere diventa maggiore del numero di protoni all'interno del nucleo. In questo caso la forza di attrazione esercitata dal nucleo viene vinta dalla forza di repulsione tra gli elettroni presenti nelle elettrosfere, con il risultato di un aumento del raggio dell'atomo. Quindi, il raggio di un anione sarà sempre maggiore del raggio del suo atomo neutro.
Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
Raggio anionico > Raggio atomico neutro
Le due situazioni presentate di seguito sono un buon esempio di ciò che accade al raggio di uno ione:
1°) Atomo di sodio neutro (11Na) e il catione di sodio (11A+)
Mentre l'atomo di sodio neutro ha undici protoni (sfere gialle) e undici elettroni (sfere rosse), il catione sodio ha undici protoni e dieci elettroni.

Modello di atomo neutro di sodio
Quando l'atomo di sodio neutro perde un elettrone, il raggio diminuisce.
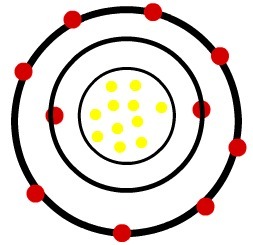
Modello di un catione di sodio
Osservazione: Il terzo livello non è stato rappresentato nell'immagine del catione perché, perdendo l'unico elettrone che aveva, si è svuotato e, quindi, è stato trascurato, ma è presente.
2°) atomo neutro di fosforo (15P) e il catione fosforo (15P-3)
Mentre l'atomo di fosforo neutro ha quindici protoni (sfere gialle) e quindici elettroni (sfere rosse), l'anione di fosforo ha quindici protoni e diciotto elettroni.
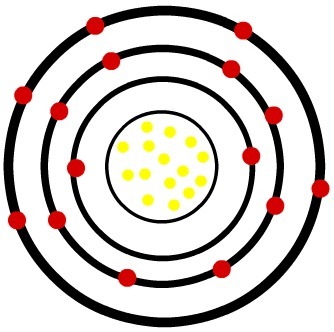
Modello di un atomo di fosforo neutro
Quando l'atomo di fosforo neutro guadagna tre elettroni, il raggio aumenta.
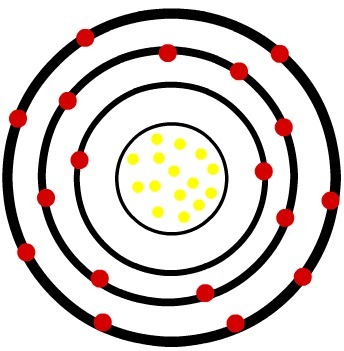
Modello di un anione del fosforo
Di Me. Diogo Lopes Dias
Vorresti fare riferimento a questo testo in un lavoro scolastico o accademico? Guarda:
GIORNI, Diogo Lopes. "raggio ionico"; Brasile Scuola. Disponibile in: https://brasilescola.uol.com.br/quimica/raio-ionico.htm. Consultato il 28 giugno 2021.


