A ammidi sono composti organici caratterizzati da presenza di a azoto (N) direttamente attaccato a un carbonile (C=O). Si tratta di sostanze disponibili in modo naturale, una di queste si trova negli escrementi dei mammiferi (urea), ma si possono ottenere anche per sintesi artificiale.
Le ammidi possono essere prodotte, ad esempio, da disidratazione del sale di ammonio, processo utilizzato nella produzione di polimeri. Sono anche usati come fertilizzanti, a causa della sua disponibilità di azoti, e come farmaco, con azione antimicrobica.
Leggi di più:Acrilammide - ammide che può essere originata dal riscaldamento di alcuni alimenti
struttura ammidica
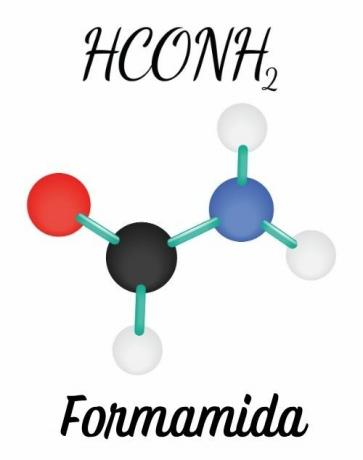
Le ammidi sono formate da a azoto legato direttamente a un gruppo carbonilico o acilico (R-C=O). Il doppio legame tra carbonio è il ossigeno e la possibilità di spostare questa coppia in azoto danno alla molecola geometria planare, a differenza delle ammine, che hanno geometria piramidale.
Classificazione delle ammidi
Classificazione in base al numero di sostituenti organici
Così come il ammine, le ammidi sono classificate secondo la numero di radicali organici sostitutivi che l'azoto possiede, invece, per le ammidi, dobbiamo considerare che uno dei leganti del gruppo sarà il gruppo acilico, cioè avremo solo ammidi del tipo:
- Ammide non sostituita: ha azoto legato a due to idrogeni e un gruppo carbonilico.
Esempio:

- Ammina monosostituita: ha azoto legato ad un idrogeno, un gruppo carbonilico e un radicale organico. In questo caso, dove uno degli idrogeni è stato sostituito da una catena di carbonio, considera R come un gruppo organico.
Esempio:

- Ammina disostituita: ha azoto legato a due radicali organici e un carbonile. In questo caso, i due idrogeni sono stati sostituiti da catene di carbonio.
Esempio:

Vedi anche: Come classificare gli alogenuri organici?
Classificazione in base al numero di carbonili legati all'azoto
Le ammidi possono anche essere classificate in base al numero di carbonili attaccati direttamente all'azoto della molecola.
- ammidi primarie: un solo gruppo acilico legato all'azoto (R-CO)NH2 .
- ammidi secondarie: due carbonili o gruppi acilici legati all'azoto (R-CO)2NH.
- ammidi terziarie: tre gruppi acilici legati all'azoto (R-CO)3No.

Nomenclatura delle ammidi
IL nomenclatura per ammidi sarà dato da:
prefisso che indica il numero di atomi di carbonio nella catena + posizione e infisso che indica insaturazioni (se presenti) + terminazione ammidica |
Vedi la tabella qui sotto:
Prefisso (n. carboni) |
Infisso (saturazione della catena) |
Suffisso (gruppo funzionale) |
|||
1 carbonio |
Incontrato- |
Solo chiamate singole |
-un- |
ammidi |
-ammide |
2 carboni |
Et- |
||||
3 carboni |
Puntello- |
1 doppio legame |
-it- |
||
4 carboni |
Ma- |
||||
5 carboni |
pentito- |
2 doppi legami |
-dien- |
||
6 carboni |
Esadecimale- |
||||
7 carboni |
Hept- |
1 triplo legame |
-nel- |
||
8 carboni |
ottobre- |
||||
9 carboni |
Non- |
2 collegamenti tripli |
-diin- |
||
10 carboni |
dic- |
Il conteggio del carbonio deve iniziare dal lato più vicino all'azoto del gruppo funzionale.
Esempi:
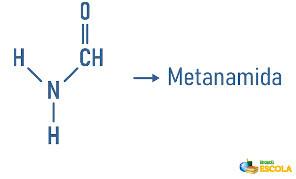



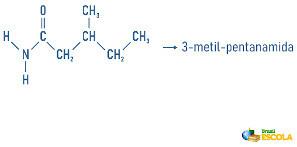
Le ammine possono anche ricevere nella loro nomenclatura una specifica sulla classificazione della molecola:
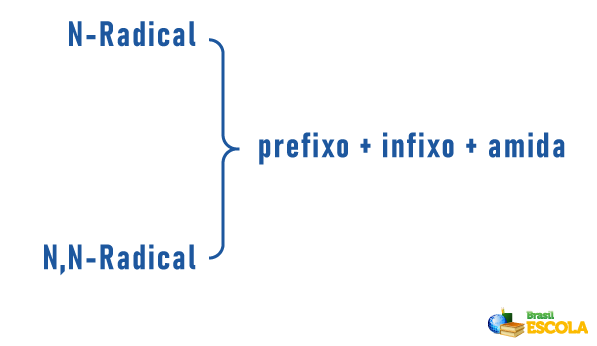
Ricordando che la nomenclatura per i radicali è formata da: Pcorreggere indicando numero di carboni + terminazione “il” o “ila”. I radicali sono posti nella nomenclatura in ordine alfabetico.
Esempi:


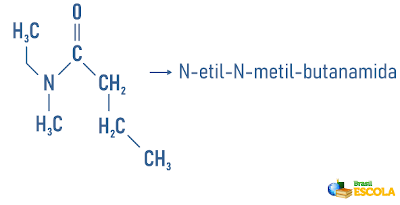
Accedi anche a: Nomenclatura degli idrocarburi ciclici e ramificati
Proprietà delle ammidi
- Elevato punto di fusione e di ebollizione, che avrà un valore graduato in base alle dimensioni e alla disposizione spaziale della catena di carbonio.
- Altamente polare per la presenza di carbonile e azoto.
- Legame idrogeno di ammidi non sostituite e monosostituite.
- Le molecole più piccole e più semplici sono solubili in acqua. La dimensione della molecola interferisce anche con la solubilità delle ammidi: più grande è la catena di carbonio, meno saranno solubili in acqua.
- Le ammidi sono basiche per la propensione a ricevere ioni H+.
Applicazione di ammidi
- Utilizzati come intermediari nella produzione di polietileni come il nylon.
- Applicato nella formulazione di farmaci quali sulfanilamide e penicillina, principi attivi di farmaci battericidi per il controllo delle infezioni.
- L'urea, che può essere ottenuta sinteticamente o come prodotto escreto dai mammiferi, è una sostanza del gruppo ammidico, una diammide. Viene utilizzato come integratore alimentare in agricoltura e come fertilizzante.

Ottenere le ammidi
Le ammidi si trovano facilmente in forma naturale, ma la loro forma sintetica è ancora ampiamente utilizzata nei processi industriali. Di seguito sono riportate alcune reazioni di produzione di ammidi basate su altri composti azotati.
Reazione di disidratazione del sale di ammonio

Reazione delle ammine con cloruro acido
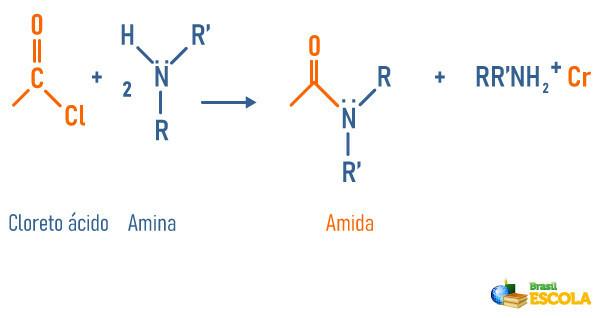
-
Reazione di anidridi con ammine
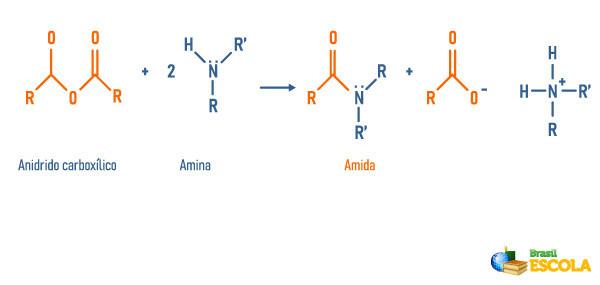
Reazione degli esteri con le ammine

Riarrangiamento strutturale di un'aldossima
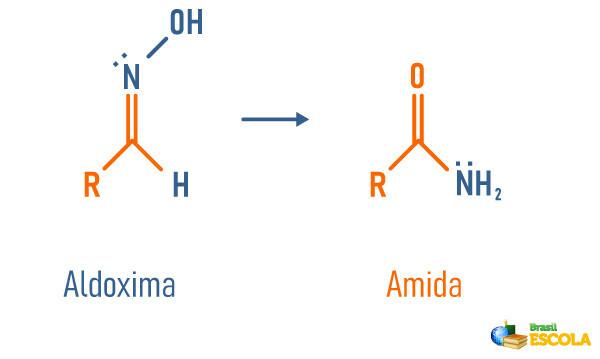
-
Idratazione di nitrile
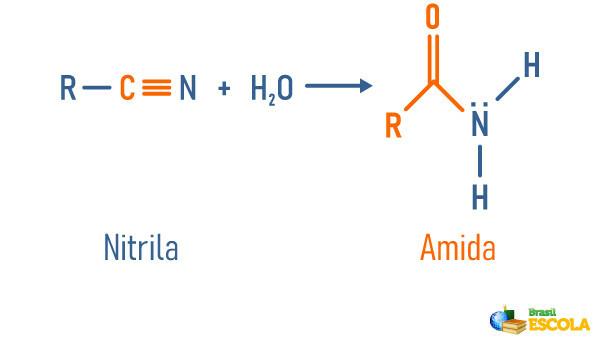
Leggi anche: Idrolisi ammidica - reazione utilizzata per ottenere sostanze importanti
esercizi risolti
Domanda 1 - (UFRS) L'aspartame, nella foto sotto, è un dolcificante artificiale utilizzato in molte bevande analcoliche e alimenti a basso contenuto calorico.

Il gruppo inquadrato nella figura è caratteristico della funzione organica
A) estere.
B) ammide.
C) amminoacido.
D) ammina.
E) carboidrati.
Risoluzione
Alternativa B. Il gruppo funzionale selezionato in figura è un'ammide, per la presenza di un carbonile (C=O) legato direttamente all'azoto (N).
Domanda 2 - (UNESP) Nell'agosto 2005 è stato segnalato il sequestro di lotti di lidocaina che avrebbero causato la morte di diverse persone in Brasile, a causa di problemi di fabbricazione. Questo farmaco è un anestetico locale ampiamente utilizzato negli esami endoscopici, riducendo il disagio del paziente. La sua struttura molecolare è mostrata di seguito:
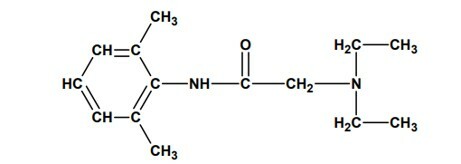
e presenta le funzioni:
A) ammina secondaria e ammina terziaria.
B) ammide e ammina terziaria.
C) ammide ed estere.
D) estere e ammina terziaria.
E) estere e ammina secondaria.
Risoluzione
Alternativa B.
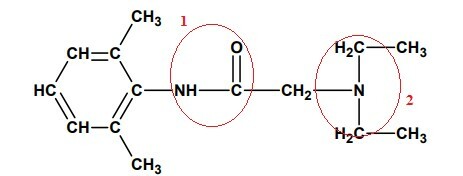
Dopo aver selezionato e numerato le parti caratteristiche di ciascuna funzione organica, analizziamo ciascuna di esse:
1- È un AMIDA per la presenza del gruppo acilico, (R-C=O) direttamente legato all'azoto, monosostituito.
2- Poiché non abbiamo la presenza del gruppo acilico (R-C=O), ma solo l'azoto legato direttamente ad altri atomi di carbonio di questo gruppo abbiamo un'AMINA TERZIARIA, perché tutti e tre gli idrogeni, precedentemente legati all'azoto, sono stati sostituiti da gruppi Organico.
Di Laysa Bernardes Marques de Araújo
Insegnante di chimica