voi metalli sono elementi chimici che hanno come caratteristica fisica principale la capacità di perdere elettroni e, di conseguenza, formare cationi metallici. Per questo motivo possono formare due tipi di legami chimici: il legame ionico e il legame legame metallico.
IL legame ionico si verifica quando un metallo interagisce con un elemento di natura metallica, che può essere a ametal o idrogeno. In questo tipo di legame, abbiamo la perdita di elettroni da parte dei metalli e l'acquisizione di elettroni da parte dei non metalli o dell'idrogeno.
già il legame metallico si stabilisce tra gli atomi di un singolo elemento metallico. Questo tipo di legame si verifica solo tra gli atomi di un singolo metallo ed esclusivamente perché un metallo non può stabilire un legame chimico con un altro elemento metallico diverso.
Caratteristiche generali dei metalli
Solidi a temperatura ambiente, ad eccezione del mercurio;
Sono brillanti;
Hanno alti punti di fusione e di ebollizione;
Sono generalmente di colore argento, ad eccezione dell'oro, che è dorato, e del rame, che è rossastro;
I metalli puri sono formati da gruppi di atomi (di un singolo elemento chimico) chiamati reticoli cristallini.
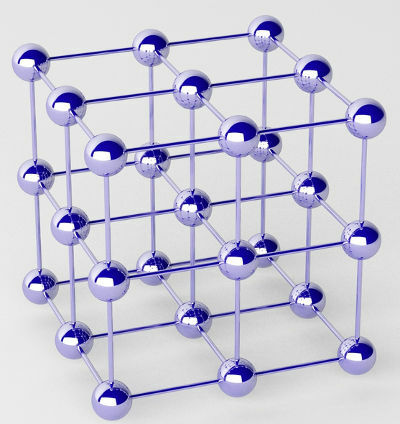
Rappresentazione del reticolo cristallino di un metallo
Principi dell'incollaggio metallico
A legame metallico, i reticoli cristallini che formano i metalli sono in realtà un cluster ionico (composto solo da cationi ed elettroni). Gli elettroni presenti nello strato di valenza degli atomi di metallo vengono delocalizzati, cioè lasciano lo strato di valenza, facendo diventare l'atomo un catione (carente di elettroni).
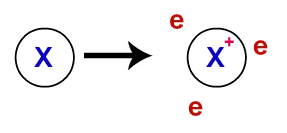
Rappresentazione di elettroni delocalizzati dal guscio di valenza
Dopo essere stati delocalizzati, gli elettroni degli atomi metallici iniziano a circondare i cationi, formando un vero "mare di elettroni". Ciascuno degli elettroni presenti in questo mare ha la capacità di muoversi liberamente attraverso il reticolo cristallino del metallo.

Rappresentazione del modello marino elettronico electron
NOTA: Gli elettroni "dal mare" non sono in grado di lasciare il reticolo cristallino e attraversarlo.
Proprietà dei metalli giustificate dal legame metallico
a) Malleabilità
Attraverso un metallo è possibile produrre lamiere di diversi spessori e lamiere. È grazie a questa proprietà dei metalli che possiamo costruire vari oggetti, come coltelli, spade, ecc.

La lama di una spada è fatta di metallo
b) Conducibilità
I metalli, in generale, sono buoni conduttori di corrente elettrica e calore. Quando un qualsiasi metallo è in contatto con una fonte di calore o una fonte di corrente elettrica, è in grado di condurli.

Una padella di alluminio nella fiamma di un fornello diventa completamente calda a causa della conduttività.
c) Duttibilità
Attraverso un metallo, possiamo produrre fili. L'uso di un metallo sotto forma di fili ne facilita l'uso, soprattutto in relazione alla conduttività elettrica.

Un metallo, come il rame, può essere utilizzato per produrre fili.
Di Me. Diogo Lopes Dias
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ligacao-metalica.htm
