Alcuni composti non hanno bisogno di avere otto elettroni nel guscio di valenza per raggiungere la stabilità, quindi sono considerati eccezioni alla regola dell'ottetto. Scopri ora perché alcuni elementi sfuggono all'obbligo di avere un ottetto di elettroni nell'ultimo guscio.
Berillio (Essere)
È un'eccezione alla regola dell'ottetto perché è in grado di formare composti con due singoli legami, quindi si stabilizza con solo quattro elettroni nel guscio di valenza. 
Poiché l'idrogeno (H) ha bisogno di cedere due elettroni per formare il legame (H - Bene - H), l'atomo di berillio (Be) condivide i suoi elettroni e raggiunge la stabilità.
Alluminio (Al)
È un'eccezione alla regola dell'ottetto perché raggiunge la stabilità con sei elettroni nel guscio di valenza. L'atomo di alluminio tende a cedere i suoi elettroni e quindi può formare tre singoli legami con altri atomi: 
In questo caso, l'alluminio (Al) ha formato tre legami con tre atomi di fluoro (F).
Boro (B)
Forma sostanze molecolari con tre singoli legami.
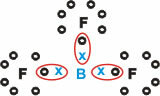
Si noti che il boro (B) tende a donare i suoi elettroni agli atomi di fluoro (F), che obbediscono alla regola dell'ottetto, richiedendo otto elettroni nel guscio di valenza. Quando il boro cede i suoi elettroni, il fluoro si stabilizza con l'ottetto formato.
di Liria Alves
Laureato in Chimica
Squadra scolastica brasiliana
Vedi altro!
Teoria dell'ottetto
Chimica generale - Chimica - Brasile Scuola
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/quimica/excecoes-regra-octeto.htm