l'entropia è a grandezzatermodinamica Associato a irreversibilità degli stati di un sistema fisico. È comunemente associato al grado di "disturbo" o "casualità” di un sistema. Secondo una delle dichiarazioni di 2° Legge della Termodinamica:
“In un sistema termicamente isolato, la misura dell'entropia deve sempre aumentare nel tempo, fino a raggiungere il suo valore massimo”.
In altre parole, il entropia è in grado di misurare il significato di "freccia del tempo” di un sistema. Quando vediamo le immagini sottostanti, sappiamo intuitivamente che lo stato iniziale del sistema è rappresentato dall'immagine del sinistra, dei più grandi organizzazione:
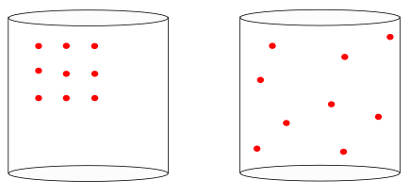
Guardando l'immagine precedente, sappiamo che la configurazione finale più probabile è quella in cui gli atomi hanno velocità in tutte le direzioni, così come posizioni casuali. Ecco cos'è l'entropia: a molteplicità degli stati di un sistema deve sempre aumentare.
Esempi
Quale delle seguenti impostazioni è più probabile da osservare per una disposizione dei mattoni nel tempo?

Nella prima configurazione, il molteplicità degli stati dei blocchi è poco: sono tutti disposti nel direzioneorizzontale, parallelo l'un l'altro. Con il passare del tempo o l'azione di un agente, si prevede che la sua configurazione Cresci nel numero nel stati, favorendo il Lunediconformazione, illustrato nell'immagine a destra. Si possono fare altri esempi:
Quando si mette una borsa del ghiaccio in un contenitore con più grandetemperatura, la sua temperatura aumenta fino a raggiungere il equilibrio termico. A quel punto il ghiaccio può sciogliersi. Prendendo di nuovo calore dal blocco di ghiaccio, che ora è nello stato liquido, può ridiventare solido, ma la sua conformazione non avrà la stessa organizzazione quello precedentemente presentato.
Quando si apre una bottiglia di profumo, il calore può aiutare diffusione del tuo molecole, spargendo il contenuto del profumo su tutta la lunghezza di una stanza. Non ci si può aspettare il contrario, poiché la rimozione del calore non favorirebbe il ritorno delle molecole nel pallone.
Definizione matematica di entropia
IL definizione matematica di entropia è data dal rapporto tra la quantità di calore (Q) trasferito tra due porzioni di un sistema termicamente isolato, in joule (J), per la sua temperatura assoluta, in Kelvin (K):

S = Entropia (J/K)
Q = Quantità di calore (J)
T = Temperatura assoluta (K)
La definizione data sopra è valida per processi isotermici, cioè in cui vi sono scambi termici talmente piccoli (o lenti) da non poter modificare la temperatura dell'impianto. La definizione di entropia è quindi infinitesimale (parte infinitamente piccola).
Possiamo anche intendere il concetto di entropia come segue: essendo un sistema formato da due porzioni dello stesso gas, in tante differentitemperature, è possibile estrarre una certa quantità di lavoro di lui che si muove un po' pistone o manovella, per esempio. Tuttavia, col tempo, le parti di questo gas tenderanno a equilibriotermico. Se non c'è più differenza di temperatura, anche con tutta l'energia presente, non sarà possibile estrarne nessuna lavoroutile da lui.
Di Rafael Hellerbrock
Laureato in Fisica
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/o-que-e/fisica/o-que-e-entropia.htm


