Ossidazione energetica in alchini è una reazione organica che si verifica quando un alchino (un idrocarburo che ha un triplo legame tra due atomi di carbonio) viene aggiunto a una soluzione acida con il reagente di baeyer (Permanganato di potassio - KMnO4).
NOTA: una reazione di ossidazione energetica può essere eseguita con dicromato di potassio (K2Cr2oh7), e non solo permanganato di potassio.
Ogni volta che una reazione da si effettua l'ossidazione energetica in alchini, i prodotti che si possono originare sono acidi carbossilici, acqua (l'unico elemento che compare in ognuno di essi) e anidride carbonica (CO2).
Reagente Baeyer in ambiente acido
Quando il reagente di Baeyer viene miscelato con acqua, in presenza di a acido (sostanza in grado di rilasciare ioni H+), si ha la formazione di due ossidi (ossido di potassio e ossido di manganese II) e ossigeni nascenti ([O]).

Meccanismi di ossidazione dell'energia negli alchini
1° meccanismo: rompere il triplo legame.
Inizialmente, il triplo legame viene attaccato dagli ossigeni nascenti formati dal reagente di Baeyer. Questo attacco provoca la rottura completa del triplo legame.
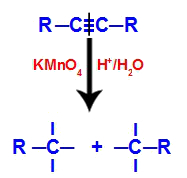
Rottura del triplo legame per attacco di ossigeni nascenti
Quando il triplo legame viene rotto, l'alchino viene diviso in due parti. Su ciascuno dei carboni che erano tripli legami, appaiono tre valenze libere.
2° meccanismo: Interazione dei gruppi ossidrile
Ognuna delle valenze libere sui carboni dove era il triplo legame è occupata da gruppi ossidrile (OH), formando un poliolo (alcol con più ossidrili).
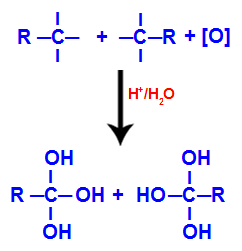
Formazione di poliolo con gruppi ossidrilici dopo la scissione del triplo legame
NOTA: Se il carbonio dove si trovava il triplo legame ha un atomo di idrogeno attaccato ad esso, quell'atomo di idrogeno riceverà un ossigeno nascente e formerà anche un altro ossidrile.
3° meccanismo: Formazione di molecole d'acqua
Quando un carbonio ha due o più gruppi OH, diventa una struttura molto instabile a causa della presenza di estremamente elettronegativi. Pertanto, a causa dell'instabilità, la molecola subisce un'autodisidratazione, cioè un idrossile si lega all'idronio (H+) da un altro ossidrile e forma acqua.

Formazione di molecole d'acqua da due ossidrili presenti nel poliolo formatosi
4° meccanismo: Formazione del prodotto
Dopo la formazione di molecole d'acqua, il carbonio perde un legame a causa dell'uscita di a idrossile, e anche l'ossigeno dell'altro ossidrile perde un legame che si stava formando con idrogeno. Pertanto, tra questo carbonio e l'ossigeno, appare un doppio legame, che forma un carbonile (C=O) e stabilizza entrambi.
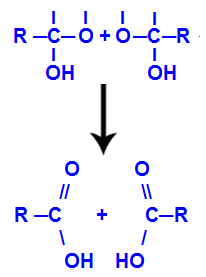
Formazione di carbonile nelle due strutture ottenute da alchine
Esempio di un'equazione di ossidazione dell'energia degli alchini
Esempio: Ossidazione energetica di But-1-ino
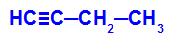
Formula di struttura di but-1-yne
Quando but-1-yne viene posto in un mezzo contenente il reagente di Bayer, acqua e acido, il legame si rompe. triplo esistente tra i carboni 1 e 2, per l'attacco degli ossigeni nascenti esistenti nel mezzo, come nell'equazione sotto:
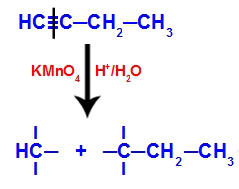
Rottura delle connessioni but-1-yne
Dopo la rottura del triplo legame, i atomi di carbonio 1 e 2 ricevono tre ossidrili, ma il carbonio 1 ne avrà uno in più perché aveva un atomo di idrogeno (che si lega ad un ossigeno nascente), formando due polioli (frammento 1 e 2).

Equazione che rappresenta la formazione di polioli
Poco dopo, poiché i polioli sono instabili, si ha la formazione di molecole d'acqua dagli idrossili. Nel frammento 1 compare una molecola d'acqua (perché ci sono tre ossidrili) e, nel frammento 2, compaiono due molecole (perché ci sono quattro ossidrili).
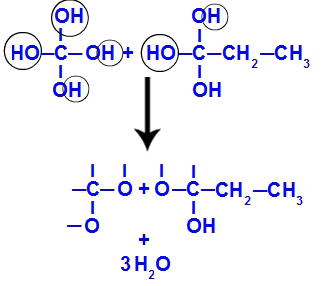
Formazione di molecole d'acqua da frammenti but-1-ino
Infine si ha la formazione del doppio legame tra i carboni che hanno perso ossidrile e gli ossigeni che hanno perso idrogeno, che dà origine ai carbonili.

Formazione di carbonili nei frammenti but-1-ino
Con l'equazione sopra, possiamo vedere che but-1-yne ha dato origine a un acido carbossilico e anidride carbonica (CO2).
Di Me. Diogo Lopes Dias
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/quimica/oxidacao-energetica-alcinos.htm
