ILosmosi e il passaggio del solvente, da una soluzione meno concentrata ad una soluzione più concentrata, attraverso a membrana semipermeabile, fino a quando la pressione esercitata dalla soluzione sulla membrana impedisce il passaggio del solvente. Questo processo ha lo scopo di bilanciare la concentrazione della soluzione.
Leggi anche tu: Soluto e solvente
pressione osmotica
IL pressione osmotica e il pressione esercitata sulla soluzione con maggiore concentrazione in modo che non si verifichi osmosi, cioè che il solvente non attraversi la membrana semipermeabile.
La pressione osmotica viene utilizzata nei processi di desalinizzazione dell'acqua, forzando il processo di osmosi inversa, facendo passare il solvente dalla soluzione più concentrata a quella meno concentrata. Chiamiamo questo processo osmosi inversa. Vedere l'immagine seguente che confronta i due processi:
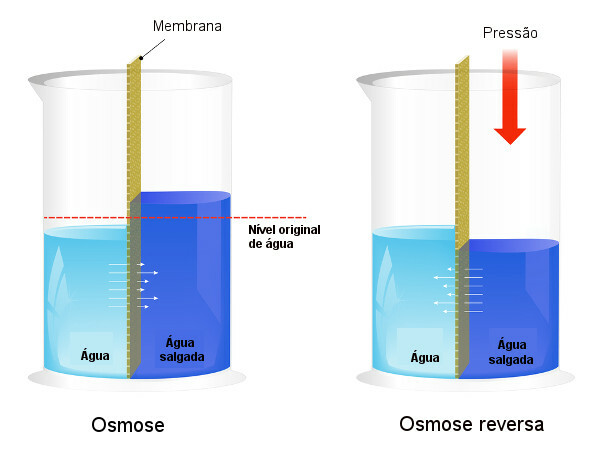
Si noti che, in osmosi, il passaggio del solvente è in direzione della soluzione più concentrata e che, in osmosi inversa, il passaggio è in senso opposto, a causa della pressione applicata. Per approfondire l'argomento, leggi il nostro testo:
pressione osmotica.saperne di più: Osmosi inversa nella desalinizzazione dell'acqua di mare
equazione della pressione osmotica
Pressione osmotica, rappresentata dalla lettera pi (π) di una soluzione, si calcola con la seguente equazione:
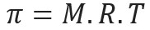
M = concentrazione in mol/L
R = costante universale dei gas perfetti
T = temperatura assoluta, in K
come gli altri proprietà colligative, la pressione osmotica dipende da concentrazione della soluzione, cioè, maggiore è la concentrazione della soluzione, maggiore è l'effetto dell'osmosi sulle soluzioni e, quindi, maggiore è la pressione osmotica.
Esempi
L'osmosi appare nella nostra vita quotidiana in momenti diversi. Possiamo citare l'esempio di processo di salatura della carne alla tua conservazione. voi microrganismi che causerebbe la degradazione della carne perdere acquadall'interno verso l'esterno, che ha una concentrazione di sale, che fa durare più a lungo il cibo.
A causa del sale, capita anche che il le foglie di insalata appassiscono per aver perso acqua dall'interno del loro cellule (un po' meno concentrato) per il soluzione temperata nell'ambiente esterno.
Anche l'osmosi è importante quando si parla di sangue umano. Diciamo che il Globuli rossi e il sangue è uno mezzo isotonico, cioè hanno la stessa pressione osmotica, permettendo l'ingresso e l'uscita dell'acqua dalla cellula con facilità.
Tuttavia, quando il sangue diventa meno concentrato rispetto all'interno dei globuli rossi (mezzo ipotonico), il passaggio dell'acqua avverrà più facilmente all'interno della cellula, rendendola gonfiarsi fino a scoppiare. Se il sangue raggiunge una concentrazione maggiore della concentrazione dei globuli rossi (mezzo ipertonico), la le cellule del sangue appassiscono, in quanto perdono acqua.

Per lo stesso principio di conservazione della carne, il conservazione della fruttanelle composte di caramelle, che conservano il cibo grazie a alta concentrazione di zucchero nella soluzione.
Di seguito sono riportati altri esempi in cui si verifica l'osmosi:
- nell'aumento della linfa nei vasi conduttori della pianta;
- a emodialisi;
- nel passaggio selettivo dei nutrienti nelle cellule del corpo umano.
Per capire come avviene l'osmosi nella cellula animale, nella cellula vegetale e in altri problemi biologici, leggi: Osmosi: cos'è e come si manifesta nella cellula animale e vegetale.
di Victor Ferreira
Insegnante di chimica
