IL stereoisomeria, conosciuto anche come Isomeria spaziale, è un tipo di isomeria in cui i suoi isomeri sono differenziati dai legami tra i loro atomi disposti in modo diverso nello spazio.
Esistono due tipi di stereoisomeri, i diastereoisomeri e il enantiomeri. I diastereoisomeri sono isomeri geometrici del tipo cis-trans, che non sono immagini speculari l'uno dell'altro, mentre gli enantiomeri sono isomeri ottici che sono immagini speculari l'uno dell'altro.
Parlando un po' di cis-trans diastereoisomero, si verifica solo in composti insaturi o ciclici. Perché non si verifica nei composti a catena satura, cioè che hanno solo legami singoli tra i carboni?
Può capitare di confondersi, pensando che certi composti saturi siano diastereoisomeri, quando in realtà rappresentano lo stesso composto. Ad esempio, di seguito, abbiamo tre conformazioni spaziali degli atomi di 1,2-dicloroetano:
H H H H H Cl
│ │ │ │ │ │
H — Ç — Ç — H H — Ç — Ç — ClH — Ç — Ç — H
│ │ │ │ │ │
Cl ClCl H Cl H
Sono questi tre diastereoisomeri? Non. In realtà,
le tre molecole sono dello stesso composto. Quello che succede è che i singoli legami o sigma (σ) tra i carboni possono subire rotazioni, risultando in diverse disposizioni atomiche.Guarda come questo accade nello schema seguente con l'etano:

Questi composti, che in realtà sono lo stesso composto, non svolgono isomeria geometrica cis-trans, ma sono detti isomeri conformazionali, in quanto differiscono solo per la conformazione dei loro atomi causata dalla rotazione attorno al singolo legame.
Uno dei modi per rappresentare queste molecole per facilitare la visualizzazione della rotazione dell'asse di connessione è attraverso il La proiezione di Newman, in cui si considera come se il piano di visione fosse esattamente sull'asse del legame tra i carboni e sono rappresentati da un cerchio centrale. Vedi la proiezione di Newman per l'etano:

Possiamo rappresentare queste diverse conformazioni anche attraverso il formula su cavalletti:
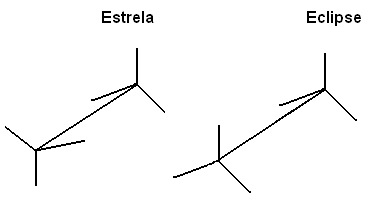
Questa libera rotazione dell'asse di collegamento non si verifica più nei composti insaturi o nei ciclici. Ad esempio, immagina di costruire un modello semplice, che rappresenti due carboni con due palline di polistirolo collegate da uno stuzzicadenti incastrato in essi.
Quando abbiamo un solo stuzzicadenti e teniamo in mano una delle palline, l'altra può facilmente ruotare attorno al proprio asse, proprio come fa con la semplice legatura.

Tuttavia, se mettiamo un altro stuzzicadenti che collega le due sfere, non saremo in grado di tenere una sfera e ruotare l'altra. Se lo facciamo, gli stuzzicadenti si romperanno. Allo stesso modo, quando c'è un legame pi e un sigma (doppio legame) c'è un impedimento alla rotazione dei carboni.
Quindi, nel caso sottostante, in cui abbiamo un doppio legame tra i carboni, non si tratta di due isomeri conformazionali, cioè due conformazioni per la stessa molecola; in realtà abbiamo due diastereoisomeri cis-trans:
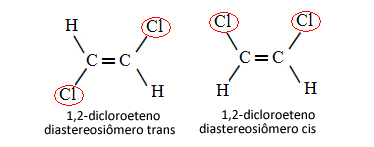
Vedi di più su questo tipo di isomeria nel testo Isomeri geometrici o cis-trans.
di Jennifer Fogaça
Laureato in Chimica
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/quimica/isomeria-conformacional.htm
