A sostanze sono quei materiali con composizione chimica costante e che hanno la loro Proprietà fisiche ben definiti, come i punti di fusione e di ebollizione e il densità, non variando in certo temperatura e pressione.
L'acqua distillata utilizzata nei laboratori, ad esempio, è un sostanza pura formato solo da molecole di H2O (questa è la sua composizione chimica costante) e, alla pressione di 1 atm (a livello del mare), avrà sempre un punto di fusione pari a 0°C, un punto di ebollizione pari a 100°C e una densità di 1,0 g /ml a 4°C. Vedi altri due esempi:
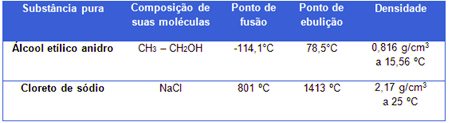
Proprietà fisiche di alcol e cloruro di sodio
Esistono due tipi di sostanze, semplici e composte:
Il) sostanze semplici
Sono quelli le cui molecole sono formate solo da un singolo tipo di elemento chimico. Gli atomi degli elementi possono presentarsi in forma isolata, essendo sostanze monoatomiche, oppure formare molecole biatomiche e triatomiche. Esempi:
Monoatomico: è il caso dell'elio gassoso (He), a gas primario che appare isolato in natura, e anche dal
ferro (Fe) e del alluminio (Al), che sono metalli. Vedi il testo Connessione metallica capire come gli atomi di questi elementi stanno insieme;Biatomici: il gas ossigeno presente nell'aria atmosferica è costituito da molecole formate ciascuna da due atomi di ossigeno, O2, e le molecole di gas idrogeno sono formate da due atomi di idrogeno, H2;
Triatomici: oh ozono è formato da tre atomi di ossigeno, O3.
B) sostanze composte
Sono quelli le cui molecole, o gruppi ionici, sono formati da due o più elementi chimici o ioni. Acqua, alcool e cloruro di sodio, sopra menzionati, sono tutti classificati come sostanze composite o composti chimici, in quanto costituiti da elementi diversi (idrogeno, ossigeno, carbonio, sodio e cloro).
Altri esempi: diossido di carbonio (CO2), monossido di carbonio (CO), metano (CH4) e ammoniaca (NH3).
Le sostanze composte possono essere scomposte in sostanze semplici. Ad esempio, quando passiamo una corrente elettrica su cloruro di sodio fuso, a reazione redox che darà origine a due sostanze semplici, sodio metallico (Na(S)) e cloro gassoso (Cl2(g)). Questo processo è noto come Elettrolisi Ignea di Cloruro di sodio.
di Jennifer Fogaça
Laureato in Chimica
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/quimica/substancias-simples-compostas.htm

