IL distillazione frazionata è un processo utilizzato per separare miscele omogenee formate da almeno due liquidi miscibili. La separazione con questo metodo si basa sui diversi punti di ebollizione dei componenti della miscela.
Questo tipo di separazione viene generalmente applicato a miscele che hanno componenti con una differenza di punto di ebollizione di circa 25 °C.
L'apparato principale per il processo è il colonna di frazionamento, detta anche colonna di distillazione, che ha al suo interno una serie di ostacoli per evitare che tutti i componenti della miscela si volatilizzino contemporaneamente.
Fondamentalmente, la miscela viene riscaldata in un pallone da distillazione fino a quando lo stato fisico del componente con il punto di ebollizione più basso cambia. Quindi il vapore passa attraverso una colonna frazionata, che separa le frazioni, dopodiché il condensatore fa ritornare la sostanza allo stato liquido in modo che venga convogliata nel contenitore di raccolta.
La distillazione frazionata è ampiamente utilizzata nelle industrie e nei laboratori, avendo un grande significato commerciale. Esempi di applicazioni sono: purificazione dell'acqua, separazione dei componenti del petrolio e separazione dell'aria liquefatta.
Il petrolio, ad esempio, è una miscela di idrocarburi, come butano (PE 20 °C), benzina (PE 150 °C) e cherosene (PE 300 °C). Pertanto, l'ordine di separazione dei componenti nella distillazione frazionata dal punto di ebollizione più basso a quello più alto è: butano, benzina e cherosene.
Attrezzatura per distillazione frazionata
Nella distillazione frazionata viene utilizzato un sistema composto dalle seguenti parti:
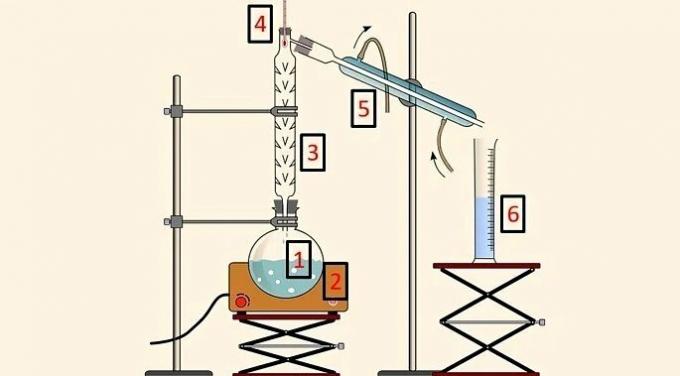
- Pallone da distillazione (1), che contiene la miscela;
- Coperta riscaldante (2), che fornisce calore alla miscela;
- Colonna di distillazione (3), che permette la separazione in funzione della temperatura;
- Termometro (4), per seguire il cambio di temperatura;
- Condensatore (5), per raffreddare il componente evaporato;
- Becher (6), per raccogliere il componente separato allo stato liquido.
Processo di separazione in distillazione frazionata
In primo luogo, la miscela viene posta nel pallone di distillazione insieme ai granuli anticollisione per evitare una rapida evaporazione.
La colonna frazionata è collegata al pallone di distillazione. Man mano che la miscela viene riscaldata, il vapore sale nella colonna, il cui interno è rivestito da "ostacoli", solitamente di perle di vetro o porcellana.
Il contatto del fluido all'interno della colonna fa sì che le sostanze della miscela perdano calore quando passano attraverso l'apparecchiatura e solo il componente con il punto di ebollizione più basso va alla sommità della colonna.
Il vapore che raggiunge il condensatore viene quindi raffreddato fino a quando non si liquefa, cioè ritorna allo stato liquido e viene raccolto nel pallone di ricezione.
Leggi anche: Cos'è la distillazione?
Distillazione frazionata del petrolio
L'olio è una miscela complessa di composti organici e i diversi componenti separati nel processo di distillazione sono chiamati frazioni. Le frazioni di petrolio sono formate da idrocarburi, come benzina, diesel, cherosene e bitume.
Le frazioni sono separate nel torre di distillazione, una colonna d'acciaio riempita di vassoi che presentano "ostacoli" per il passaggio dell'olio.
Inizialmente, l'olio viene riscaldato in una fornace e la miscela riscaldata viene alimentata sul fondo di una torre di distillazione. La temperatura della torre è più alta in basso e più bassa in alto per evitare che le frazioni più pesanti evaporino con i componenti più leggeri.
Gli idrocarburi a catena di carbonio più lunghi vengono condensati e rimossi nella parte inferiore della torre. Queste frazioni sono scure, viscose e più difficili da evaporare. Quelli a catena singola, invece, hanno punti di ebollizione più bassi e, quindi, condensano a temperature più vicine alla sommità della torre, dove vengono raccolti.
saperne di più raffinazione del petrolio.
Differenza tra distillazione semplice e frazionata
La distillazione semplice si applica quando si vuole separare un solido disciolto in un liquido. Per questo, riscaldiamo la miscela fino a quando il solvente non evapora. Questo processo è più veloce e richiede meno energia rispetto alla distillazione frazionata.
Un esempio di una miscela che può essere separata per semplice distillazione è l'acqua e il sale. L'acqua, avendo un punto di ebollizione molto inferiore al sale da cucina, viene evaporata quando si scalda la miscela e, dopo essere passata in un condensatore, viene raccolta in un altro recipiente.
La distillazione frazionata viene applicata alla separazione di liquidi miscibili tra loro, come acqua e acetone.
Acquisisci maggiori conoscenze con i contenuti:
- Distillazione semplice e frazionata
- Separazione della miscela
- Esercizi di separazione delle miscele
Riferimenti bibliografici
MARRONE, T. L.; LEMAY JR., H. E.; BURSTEN, B. E.; BURGE, J. R. La chimica la scienza fondamentale. 9a ed. Pearson Prentice Hall do Brasil, 2008.
USBERCO, J.; SALVADOR, E. Chimica generale. 12a ed. San Paolo: Saraiva, 2006.
RUSSELL J B. Chimica generale. vol. 1. Makron, 1996.
- Distillazione
- Distillazione semplice e frazionata
- raffinazione del petrolio
- Esercizi di separazione delle miscele
- Separazione delle miscele
- Materiali utilizzati nel laboratorio di Chimica
- vetreria da laboratorio
- Esercizi di chimica organica con risposte