L'isomerismo di compensazione o metamerismo è un tipo di isomeria piatta, cioè la differenza tra gli isomeri può essere identificata analizzando la formula strutturale piatta della molecola.
La parola "metameria" deriva da obbiettivo, che significa "cambiamento", e semplice, che significa "parti". In questo tipo di isomeria accade esattamente questo: un cambiamento di posizione in una parte della molecola, e questa "parte" è la eteroatomo.
L'eteroatomo è qualsiasi elemento chimico che appare in una catena di carbonio tra due atomi di carbonio.
Così, abbiamo che, nell'isomero di compensazione o nel metamerismo, gli isomeri si differenziano per la posizione dell'eteroatomo nella catena.. Ciò significa che è un tipo speciale di isomeria di posizione.
È importante notare che questi isomeri hanno lo stesso gruppo funzionale e lo stesso tipo di catena. (normale o ramificato, aperto o chiuso e sarà sempre eterogeneo, per la presenza del eteroatomo).
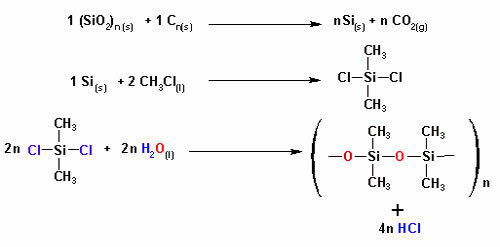
Generalmente, gli eteroatomi che appaiono attaccati al carbonio nei composti organici sono ossigeno, azoto e zolfo. Pertanto, il metamerismo si verifica normalmente in eteri, esteri, tioeteri, ammine (monosostituite o disostituite) e ammidi.
Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
Vedi sotto per due esempi di come ciò si verifica con eteri a catena aperta e chiusa:
- I due composti sottostanti hanno la stessa funzione (etere), la stessa formula molecolare (C4H10O) e lo stesso tipo di catena (aperta, normale ed eterogenea), ma differiscono perché l'ossigeno si trova in posizioni diverse. Nella prima molecola si trova tra i atomi di carbonio 1 e 2 e nella seconda tra i atomi di carbonio 2 e 3:
H3C oh CH2 CH2 CH3 H3C CH2 ─ oh CH2 CH3
metossipropano etossietano
Questo cambiamento sembra piccolo, ma cambia completamente le proprietà e le applicazioni di questi composti. Ad esempio, il metossipropano viene utilizzato nelle sintesi industriali, mentre l'etossietano viene utilizzato come anestetico comune (etere).
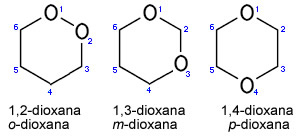
- Di seguito sono riportati tre metameri di diossano, si noti che sono tutti dieteri ciclici con catene esagonali, l'unica differenza strutturale è la posizione degli eteroatomi.
di Jennifer Fogaça
Laureato in Chimica
Vorresti fare riferimento a questo testo in un lavoro scolastico o accademico? Guarda:
FOGAÇA, Jennifer Rocha Vargas. "Isomeria di offset o metamerismo"; Brasile Scuola. Disponibile in: https://brasilescola.uol.com.br/quimica/isomeria-compensacao-ou-metameria.htm. Consultato il 27 giugno 2021.
Chimica
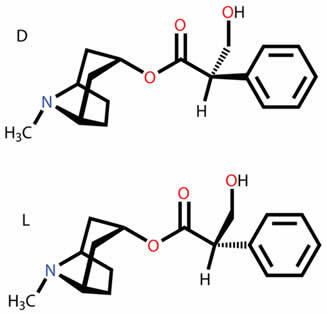
Conoscere i vari tipi di isomeri piani e spaziali, come funzione, posizione, catena, tautomerismo, metamerismo, isomeria geometrica e ottica cis-trans.