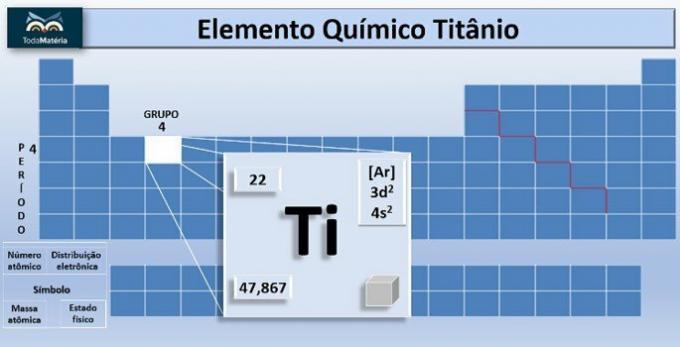
o titanio è l'elemento chimico di simbolo Ti e numero atomico, cioè numero di protoni pari a 22. Questo metallo si trova nel gruppo 4 e 4 della tavola periodica.
La massa atomica dell'elemento è 47,867 u, e poiché ha 22 elettroni negli elettroni dell'atomo, la sua distribuzione di elettroni è 1s2 2s2 2p6 3s2 3p6 4s2 3d2.
Il titanio ha proprietà desiderabili per numerose applicazioni in quanto è resistente come l'acciaio e molto più leggero.
Essendo un metallo duttile, refrattario, resistente alla corrosione, presenta resistenza meccanica, stabilità termica e bassa reattività, viene aggiunto alle leghe metalliche in modo che abbiano un elevato prestazione. La sua biocompatibilità e atossicità lo rendono utile anche per la realizzazione di protesi ossee.
Le principali caratteristiche del titanio sono:
- Punto di fusione: 1668 °C
- Punto di ebollizione: 3287 °C
- Densità: 4,5 g/cm3
- Colore: grigio argento
- Stato fisico a 20 °C: solido
- Isotopi: Ti46, voi47, voi48, voi49 e tu50
Questo elemento chimico fu scoperto dall'inglese William Gregor nel 1791 e il suo nome, derivato dal greco
titani, è stato successivamente attribuito da Martin Heinrich Klaproth.Il titanio è il nono elemento più abbondante sul pianeta e si trova nella crosta terrestre in minerali come il rutilo (TiO2) e ilmenite (FeTiO3). Pertanto, l'estrazione mineraria è il metodo principale per ottenere questo metallo.
A cosa serve il titanio?
Poiché è chimicamente non reattivo a temperatura ambiente, facilmente modellabile, ha un'elevata resistenza meccanica e alla corrosione, il titanio è usato come metallo strategico.
Le industrie aeronautiche e aerospaziali sono i principali utilizzatori del titanio per la produzione di parti, come componenti di turbine e fusoliere. Altre applicazioni sono la produzione di protesi dentarie, impianti chirurgici e gioielli.
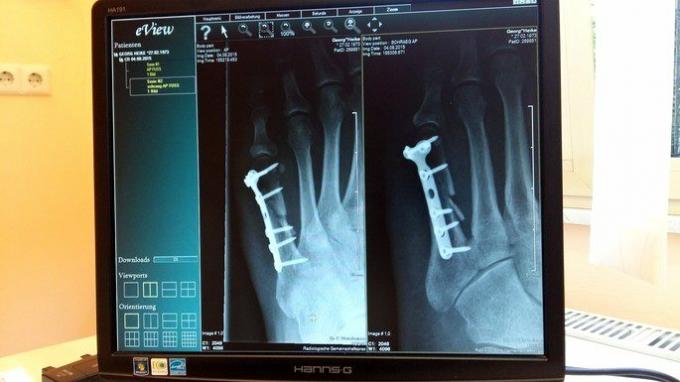
In medicina, il titanio è molto utile per la sua compatibilità con i tessuti umani, leggerezza e resistenza. Viene utilizzato per la produzione di impianti per parti del corpo, come viti di fissaggio, protesi dell'articolazione del ginocchio, protesi dell'omero, protesi dell'anca, tra gli altri.
Biossido di titanio (TiO2) è uno dei principali composti di questo elemento, essendo usato come agente sbiancante. Generalmente, gli inchiostri bianchi di alta qualità lo utilizzano per migliorare l'aspetto visivo del colore e della lucentezza. Anche altri prodotti, come dentifrici e creme solari, utilizzano il pigmento. C'è anche l'applicazione come colorante alimentare aggiunto in latticini, dolci e bevande.
In architettura, possiamo vedere l'uso del titanio per rivestire strutture curve al Museo Guggenheim di Bilbao, nel nord della Spagna.

Nella vita di tutti i giorni possiamo trovare numerosi prodotti che hanno il titanio nella loro composizione, come telai per biciclette, occhiali da vista e racchette da tennis.
Nell'industria chimica, il titanio è usato come catalizzatore per le reazioni. In questo modo è possibile controllare la velocità di reazione e ridurre i tempi di formazione del prodotto senza intaccare la composizione delle sostanze.
L'industria automobilistica ha studiato l'incorporazione del titanio nella produzione di automobili per ridurne la massa e, quindi, ridurre il consumo di carburante e aumentare la loro accelerazione.
Acquisisci maggiori conoscenze con i contenuti:
- Elementi chimici
- Tavola periodica
- Cosa sono i metalli?
Riferimenti bibliografici
ATKINS, PW; JONES, L. Principi di chimica: mettere in discussione la vita moderna e l'ambiente. 3.ed. Porto Alegre: Bookman, 2006.
FELTRE, R. Fondamenti di chimica: vol. separare. 4a ed. San Paolo: Moderna, 2005.
Lee, J. D. Chimica inorganica non così concisa. Traduzione della 5a ed. Inglese. Editore Edgard Blucher Ltd. 1999.


