| IL diffusione di un gas è un movimento spontaneo di un gas attraverso un altro, cioè la sua diffusione in un altro mezzo gassoso. |
Questa miscela di gas dà origine a miscele omogenee o soluzioni gassose. Ad esempio, i gas che escono dalle ciminiere delle fabbriche o dagli scarichi delle auto si diffondono nell'aria atmosferica e, con il passare del tempo, non siamo più riusciti a distinguerli, in quanto vi era una diffusione di questi gas attraverso il aria.

I gas emessi dai camini sono diffusi e “persi” nell'aria atmosferica, perché il volume dell'aria è molto maggiore di quello dei fumi.
| IL versamento di gas è un particolare tipo di diffusione, in cui vi è fuoriuscita di gas attraverso piccoli fori (o pareti porose, che è un insieme di piccoli fori). |
Ad esempio, i palloncini venduti ai bambini sono pieni di gas elio. Nel tempo, questo gas finisce per passare attraverso i pori di gomma del pallone, cioè c'è il suo versamento. Lo dimostra il fatto che il palloncino si sgonfia dopo poche ore.
Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
Il chimico scozzese Thomas Graham, nel 1829, studiò questo comportamento dei gas. Ha concluso che la velocità con cui un gas si diffonde o si diffonde in un altro è correlata alla sua densità. Come i suoi dati sperimentali ripetuti per tutti i gas, ha creato la seguente legge che porta il suo nome:
Legge di Graham: la velocità di diffusione o effusione di un gas è inversamente proporzionale alla radice quadrata della sua densità.
Matematicamente, questa legge può essere espressa dall'equazione:
v α 
Oppure, mettendo in relazione due gas diversi, abbiamo:
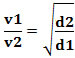
L'unità utilizzata in questo caso è il “volume che fuoriesce per unità di tempo”; quindi generalmente l/min (litri al minuto).
Pertanto, i gas con densità inferiore si diffondono più velocemente. Se è nelle stesse condizioni di temperatura e pressione, puoi anche fare una relazione di questo con la massa gas molare: maggiore è la densità del gas, maggiore è la sua massa molare e minore è la sua velocità di diffusione; e viceversa. Quindi, abbiamo:
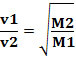
di Jennifer Fogaça
Laureato in Chimica
Squadra scolastica brasiliana
Vorresti fare riferimento a questo testo in un lavoro scolastico o accademico? Aspetto:
FOGAÇA, Jennifer Rocha Vargas. "Diffusione ed Effusione di Gas"; Brasile Scuola. Disponibile in: https://brasilescola.uol.com.br/quimica/difusao-efusao-dos-gases.htm. Consultato il 27 luglio 2021.