è chiamato Modello Rutherford la proposta per l'atomo fatta dallo scienziato Ernest Rutherford nel 1911, con lo scopo di dimostrare la forma e la composizione idealizzate del costituente della materia: il atomo.
oh Modello Rutherford è comunemente noto come il modello del sistema solare, in quanto la sua struttura e il suo funzionamento sono stati paragonati al rapporto tra il sole ei pianeti che gli ruotano attorno.
Nel suo modello, Rutherford ha paragonato il sole al nucleo dell'atomo, e gli elettroni dell'atomo sono stati paragonati ai pianeti del sistema solare, come si può vedere nella seguente rappresentazione:
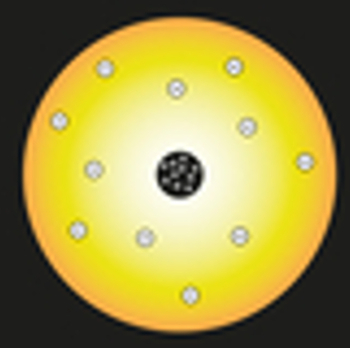
Rappresentazione del modello atomico di Rutherford
All'interno del nucleo sarebbero posizionate particelle cariche positivamente, chiamate protoni (scoperte da Eugen Goldstein). Questo nucleo sarebbe piccolo e denso e avrebbe la massa maggiore dell'atomo.
L'esperimento condotto da Rutherford
Tutte le proposte di Rutherford per la creazione del suo modello atomico erano il risultato di un esperimento in cui ha focalizzato fasci di radiazione alfa (provenienti da di polonio radioattivo presente in una scatola di piombo) su una sottile lamina d'oro, con una lastra metallica ricoperta di solfuro di zinco dietro e sui lati. lati. Il solfuro di zinco è un sale che, quando riceve radiazioni, brilla.
Rutherford ha poi notato che tre punti (a, b, c) in particolare brillavano durante questo esperimento:
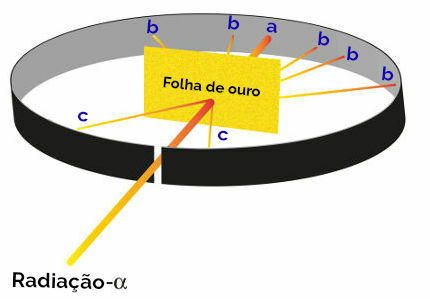
Rappresentazione dell'esperimento di Rutherford
punto a (maggiore incidenza di brillantezza): indicava che la radiazione alfa attraversava senza problemi la lamina d'oro, come sarebbe nella direzione del foro di apertura del blocchetto di piombo;
punto b (piccola incidenza di bagliore): indicava che la radiazione alfa attraversava la lamina d'oro, ma che avrebbe deviato durante l'attraversamento;
punto c (una quantità estremamente piccola di bagliore): situata di fronte alla lama d'oro, indicava che la radiazione alfa non era passata.
Rutherford ha attribuito questi risultati osservati agli atomi che formano la lamina d'oro, interpretando come segue:
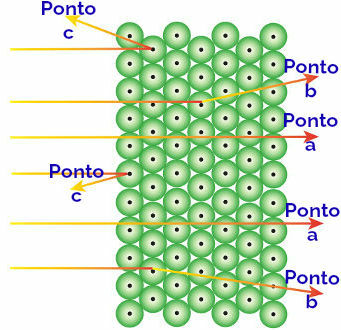
Rappresentazione del comportamento della radiazione alfa e degli atomi
Radiazione alfa che raggiunge il indicare: la radiazione alfa è positiva e attraversa una regione dell'atomo di enormi spazi vuoti. Ci sono anche elettroni presenti in alcuni orbitali.
Radiazione alfa che raggiunge il punto b: la radiazione alfa passa attraverso gli atomi della lamina d'oro, ma raggiunge un certo momento in cui passa vicino al piccolo nucleo dell'atomo, che è carico positivamente, generando repulsione nel radiazione.
Radiazione alfa che raggiunge il punto c: la radiazione alfa passa attraverso gli atomi della lamina d'oro, ma colpisce un piccolo nucleo, che si carica positivamente, generando repulsione nella radiazione.
Problematiche del modello di Rutherford
Molti fisici hanno evidenziato alcuni problemi nel modello proposto da Rutherford:
1° problema: come sarebbe possibile un nucleo con carica positiva se le particelle con carica positiva si respingono?
2° problema: perché gli elettroni nelle elettrosfere non sono attratti dai protoni nel nucleo?
3° problema: perché gli elettroni, che sono piccoli corpi in costante movimento, non perdono energia e cadono nel nucleo?
* Crediti immagine: Svic / Shutterstock
Di Me. Diogo Lopes Dias
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-modelo-rutherford.htm

