Gli idrocarburi sono composti formati solo da carbonio e idrogeno, con una formula generale: CXHsì.
Si tratta di un'ampia quantità di sostanze, le più note delle quali sono i costituenti del petrolio e del gas naturale.
La spina dorsale di un idrocarburo è costituita da carbonio e, a sua volta, gli atomi di idrogeno si legano attraverso un legame covalente.
Sono ampiamente utilizzati nell'industria chimica, essendo essenziali nella produzione di derivati del petrolio: combustibili, polimeri, paraffine, tra gli altri.
Proprietà degli idrocarburi
| interazione molecolare | Sono praticamente composti non polari e le loro molecole sono unite da un dipolo indotto. |
|---|---|
| Punto di fusione e di ebollizione | Sono bassi rispetto ai composti polari. |
| stati di aggregazione |
|
| Densità | Hanno una densità inferiore a quella dell'acqua. |
| solubilità | Sono insolubili in acqua e solubili in sostanze non polari. |
| Reattività |
|
Classificazione degli idrocarburi
Per quanto riguarda la forma della catena carboniosa principale, gli idrocarburi sono classificati in:
idrocarburi alifatici
Formata da catene di carbonio aperte o acicliche, che hanno atomi di carbonio terminali.
- alcani
- alcheni
- alchini
- alcadieni
Esempio:
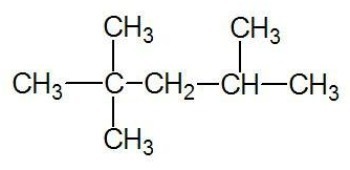
Vedi anche: catene di carbonio
Idrocarburi ciclici
Formata da catene di carbonio chiuse o cicliche che non hanno atomi di carbonio terminali.
- Ciclani
- Cicli
- ciclisti
- aromatici
Esempi:
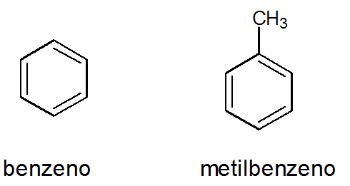
Vedi anche: benzene
Per quanto riguarda i legami delle catene di carbonio, siano essi singoli, doppi o tripli:
Idrocarburi saturi
I composti sono formati da singoli legami tra atomi di carbonio e idrogeno.
- alcani
- Ciclani
Esempio:
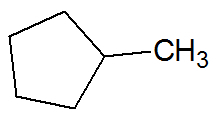
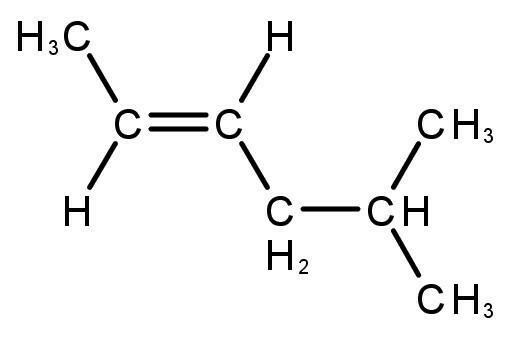
idrocarburi insaturi
I composti formati hanno doppi o tripli legami tra atomi di carbonio e idrogeno.
- alcheni
- alchini
- alcadieni
- Cicli
- ciclisti
- aromatici
Leggi anche su:
- Legami chimici
- Chimica organica
- Funzioni organiche
Nomenclatura
La nomenclatura degli idrocarburi è definita dai seguenti termini:
| PREFISSO | PROCACCIATORE D'AFFARI | SUFFISSO |
|---|---|---|
| Indica il numero di atomi di carbonio presenti nella catena. | Tipo di collegamento trovato nella stringa. | Identificazione del gruppo funzionale. |
| PREFISSO | PROCACCIATORE D'AFFARI | SUFFISSO | ||
|---|---|---|---|---|
| 1C | INCONTRATO | Solo collegamento singolo | UN | oh |
| 2C | ET | |||
| 3C | PUNTELLO | un doppio legame | IT | |
| 4C | MA | |||
| 5C | PENTA | due doppi legami | DIEN | |
| 6C | ESADECIMALE | |||
| 7C | HEPT | un triplo collegamento | NEL |
|
| 8C | OTTOBRE | |||
| 9C | NON | Due collegamenti tripli | DIIN | |
| 10C | DEC |
Esempi
Segui come si formano i nomi degli idrocarburi:
| Etano |
- Prefisso: ET, che corrisponde a 2 atomi di carbonio.
- Procacciatore d'affari: UN, che corrisponde a singoli collegamenti.
- Suffisso: oh, che corrisponde alla funzione idrocarburica.
Guarda gli altri esempi:
| Propano | |
| etene | |
| Etino | |
| propadiene |
In alcuni casi è necessario indicare la posizione del doppio o triplo legame. La numerazione deve iniziare dall'estremità più vicina di quel collegamento.
| 1,3-butadiene | |
| 1-butino |
Scopri di più su:
- Butano
- Metano
Tipi di idrocarburi
Scopri le principali tipologie di idrocarburi, le loro caratteristiche e i composti utilizzati:
alcani
Sono idrocarburi a catena aperta con legami singoli tra atomi di carbonio e idrogeno, la cui formula generale è ÇnoH2n+2.
Caratteristiche degli alcani
- Sono anche chiamate paraffine o paraffine.
- Si trovano in natura nel gas naturale e nel petrolio.
- Vengono utilizzati come combustibili: gas da cucina, benzina, gasolio, ecc.
Esempi di alcani

alcheni
Sono idrocarburi a catena aperta e hanno un doppio legame, la cui formula generale è ÇnoH2n.
Caratteristiche degli alcheni
- Sono anche chiamate olefine, alcheni o idrocarburi etilenici.
- Sono ottenuti industrialmente dal cracking di alcani presenti nel petrolio.
- Sono utilizzati come materia prima nell'industria: plastica, coloranti, esplosivi, ecc.
Esempi di alcheni

alchini
Sono idrocarburi a catena aperta con la presenza di un doppio legame, la cui formula generale è ÇnoH2n-2.
Caratteristiche degli alchini
- Sono più reattivi degli alcani e degli alcheni a causa del triplo legame.
- Gli alchini con più di 14 atomi di carbonio sono solidi.
- L'alchino più utilizzato è l'acetilene, comunemente usato nella produzione di gomme sintetiche, fibre tessili e plastiche.
Esempi di alchini

alcadieni
Sono idrocarburi a catena aperta e la presenza di due doppi legami, la cui formula generale è ÇnoH2n-2
Caratteristiche degli alcadieni
- Chiamati anche dieni o diolefine
- Si trovano in natura nei terpeni, che vengono estratti dagli oli essenziali della frutta.
- Il composto più noto è l'isoprene, che si trova nella gomma naturale e negli oli essenziali.
Esempi di alcadieni

Ciclani
Sono idrocarburi a catena chiusa con legami singoli tra atomi di carbonio e idrogeno, la cui formula generale è ÇnoH2n.
Caratteristiche dei Ciclani
- Sono anche chiamati cicloalcani o cicloparaffine.
- Sono instabili se sottoposti ad alta pressione.
- Le catene con più di 6 atomi di carbonio sono stabili, mentre le catene con meno di 5 atomi di carbonio sono reattive.
Esempi di ciclani

Cicli
Sono idrocarburi a catena chiusa con la presenza di un doppio legame, la cui formula di struttura è ÇnoH2n-2.
Caratteristiche dei cicli
- Sono anche chiamati cicloalcheni.
- I composti da 3 a 5 atomi di carbonio sono instabili.
- Di solito si trovano nel gas naturale, nel petrolio e nel petrolio.
Esempi di cicli
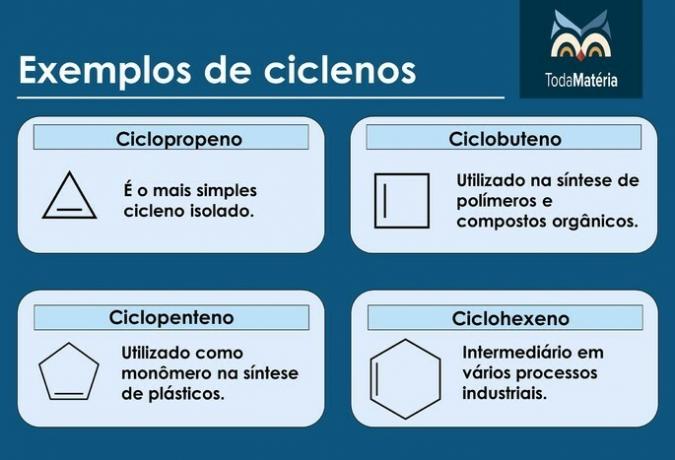
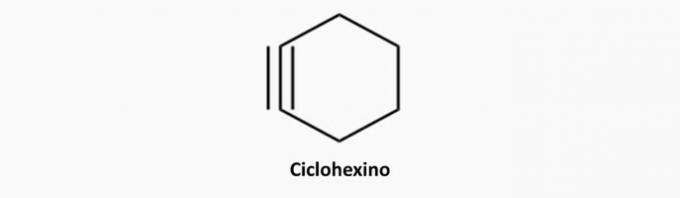
ciclisti
Sono idrocarburi a catena chiusa con la presenza di un triplo legame, la cui formula di struttura è ÇnoH2n-4.
Caratteristiche del ciclismo
- Sono anche chiamati cicloalchini o cicloalchini.
- Sono idrocarburi ciclici e insaturi.
- Sono instabili a causa del triplo legame e non si trovano in natura.
Esempi di cicline

aromatici
Sono idrocarburi a catena chiusa con legami singoli e doppi alternati.
Caratteristiche degli aromatici
- Sono anche chiamate arene.
- Sono composti insaturi, poiché hanno 3 doppi legami.
- Sono costituiti da almeno un anello aromatico.
Esempi di aromatici
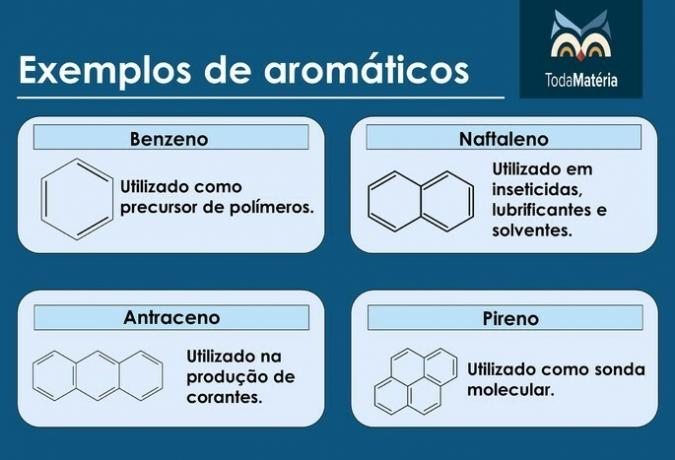
- Petrolio
- raffinazione del petrolio
- Acetilene
Riepilogo idrocarburi
| Occupazione | Formula generale |
Caratteristiche |
|---|---|---|
| alcano | Catena aperta con maglie semplici. |
|
| alchene | Catena aperta con doppio legame. | |
| alchino | Catena aperta con triplo legame. | |
| alcadiene | Catena aperta con due doppi legami. | |
| Ciclani | Catena chiusa con collegamenti semplici. | |
| Cicli | Catena chiusa con doppio legame. | |
| ciclisti | Catena chiusa con tripla maglia. | |
| Aromatico | Variabile | Catena chiusa con legami singoli e doppi alternati. |
Esercizi sugli Idrocarburi
1. (UEMA) Il GPL (gas di petrolio liquefatto), popolarmente noto anche come gas da cucina, è un combustibile fossile non rinnovabile che può esaurirsi durante la notte se non utilizzato con pianificazione e senza eccesso. È composto, tra gli altri gas, da propano C3H8, butano C4H10 e piccole quantità di propilene C3H6 e butene C4H8. Questi composti organici sono classificati come idrocarburi che hanno somiglianze e differenze tra loro. In base al tipo di legame tra i carboni e alla classificazione della catena di carbonio dei composti di cui sopra, si può affermare che:
a) i composti insaturi sono propano e butano.
b) i composti insaturi sono propene e butene.
c) i composti insaturi sono propene e butano.
d) i composti hanno catene omocicliche.
e) i composti hanno catene eterocicliche.
Alternativa b) i composti insaturi sono propene e butene.
a) SBAGLIATO. Questi composti non hanno insaturazioni, i loro legami sono semplici.
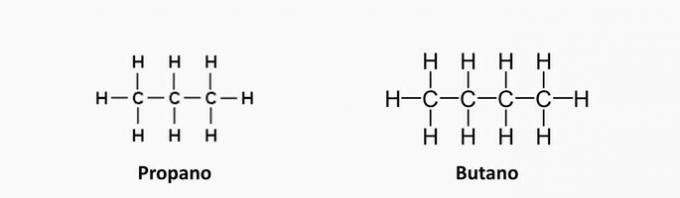
b) CORRETTO. Il termine "en" indica la presenza di doppi legami nei composti.

c) SBAGLIATO. Il butano non ha insaturazioni.

d) SBAGLIATO. Queste catene sono chiuse e gli atomi di carbonio sono legati da singoli legami.
e) SBAGLIATO. Queste catene hanno un eteroatomo, come ossigeno e azoto.

2. (Uel) Uno degli idrocarburi di formula C5H12 può avere catena di carbonio:
a) ciclico saturo.
b) aciclico eterogeneo.
c) ciclico ramificato.
d) insaturo aperto.
e) aperto ramificato.
Alternativa e) ramificata aperta.
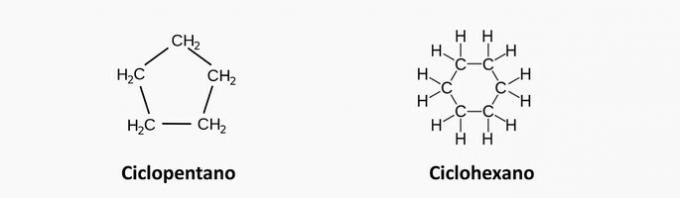
a) SBAGLIATO. Un composto ciclico saturo corrisponde a un ciclano, la cui formula è CnoH2n.
Esempio:
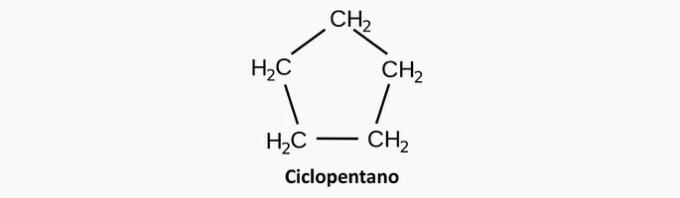
b) SBAGLIATO. Un composto aciclico eterogeneo ha la presenza di un altro elemento oltre al carbonio intercalato nella catena.
Esempio:
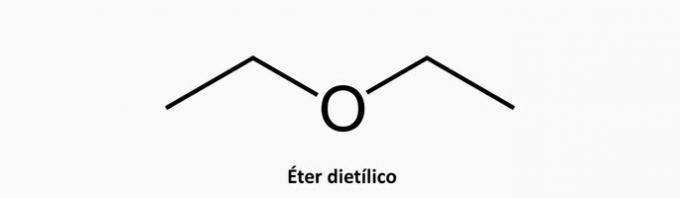
c) SBAGLIATO. Un composto ciclico ramificato ha formula CnoH2n.
Esempio:
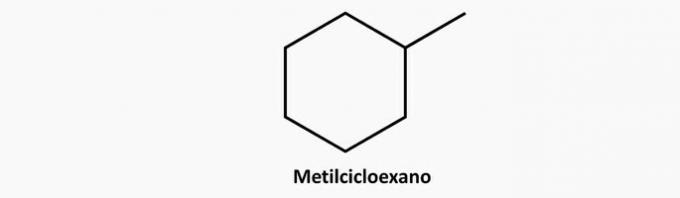
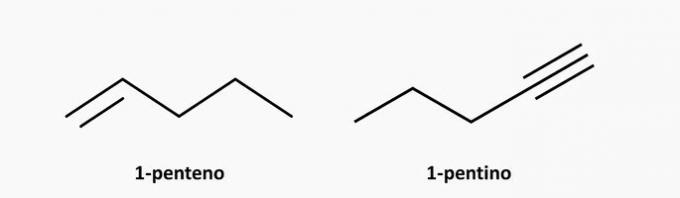
d) SBAGLIATO. Un composto insaturo a catena aperta può essere un alchene o un alchino, la cui formula è rispettivamente C.noH2n e CnoH2n-2.
Esempi:
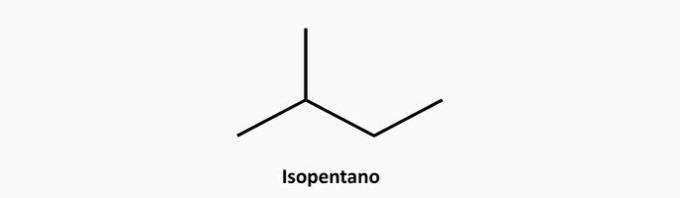
e) CORRETTO. Un composto ramificato a catena aperta è un alcano la cui formula è CnoH2n+2. Un composto di 5 atomi di carbonio e 12 idrogeni può essere isopentano.
Esempio:
3. (PUC) Gli alchini sono idrocarburi:
a) alifatici saturi.
b) aliciclici saturi.
c) alifatici insaturi a doppio legame.
d) aliciclici insaturi a triplo legame.
e) alifatici insaturi a triplo legame.
Alternativa e) Alifatici insaturi a triplo legame.
a) SBAGLIATO. I composti a catena aperta e a legame singolo sono alcani.
Esempio:

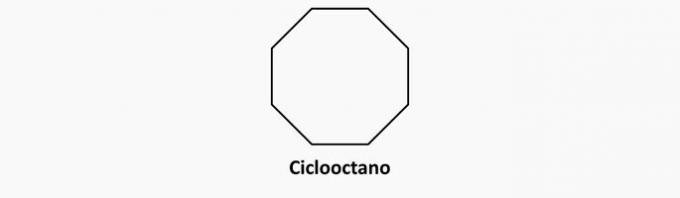
b) SBAGLIATO. I composti ciclici con legami singoli sono ciclani.
Esempio:
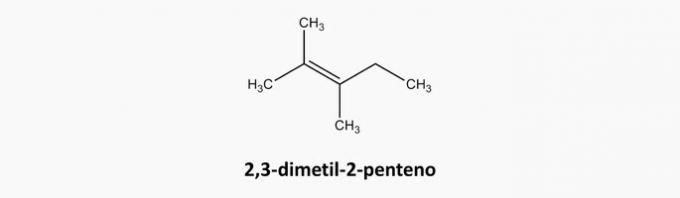
c) SBAGLIATO. I composti a catena aperta e a doppio legame sono alcheni.
Esempio:
d) SBAGLIATO. I composti ciclici e a triplo legame sono cicline.
Esempio:
e) CORRETTO. Gli alchini sono composti a catena aperta e a triplo legame.

Vuoi continuare a testare le tue conoscenze? Assicurati di controllare questi elenchi:
- Esercizi sugli Idrocarburi
- Esercizi di Chimica Organica
- Esercizi sulle funzioni organiche