A reazioni di idratazione in alcadieni sono reazioni di addizione, cioè i componenti (idronio e idrossido) della molecola d'acqua vengono aggiunti ad un alcadiene.
voi alcadieni sono idrocarburi che hanno una catena aperta e due doppi legami (formati da un sigma e un pi greco) tra i carboni, come possiamo vedere nella seguente struttura:

Formula di struttura di un alcadiene
per il reazione di idratazione negli alcadieni viene effettuata, è essenziale che il legame pi, presente nel doppio legame, sia rotto dall'influenza del calore e dell'acido solforico (H2SOLO4). Con la rottura del legame pi greco compaiono due siti di legame, ciascuno su uno degli atomi di carbonio coinvolti nel doppio legame.

Emersione di siti di legame con interruzione del legame pi
La comparsa di siti di legame sulla molecola di alcadiene è necessaria per gli ioni (H+ e oh-) dall'acqua vengono aggiunti all'alcadiene, formando, ad esempio, un dialcool (alcol con due ossidrili).
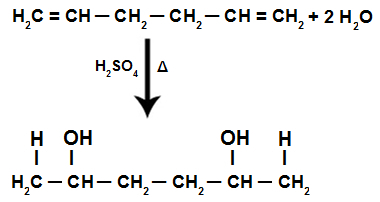
Addizione di H+ e oh- nella struttura di un alcadiene
NOTA: L'aggiunta di H+ e oh- nella struttura alcadienica segue la La regola di Markovnikov, cioè l'H+ si lega al carbonio più idrogenato e l'OH- si lega al carbonio meno idrogenato.

Esempio di applicazione della regola di Markovnikov nell'idratazione degli alcadieni
Poiché esistono diversi tipi di alcadieni rispetto alla posizione dei doppi legami, può essere che l'idratazione di un alcadiene formi composti diversi. Vedi i seguenti casi:
→ Alcadiene accumulato o condensato
È un alcadiene che ha due doppi legami che coinvolgono contemporaneamente tre atomi di carbonio, cioè non esiste un singolo legame che separa i carboni coinvolti nei legami raddoppia.

Formula di struttura di un alcadiene accumulato
Durante la reazione di idratazione di un alcadiene alternato, i legami pi sono rotti, essendo l'H+ aggiunto ai carboni più idrogenati e agli OH- aggiunto ai carboni meno idrogenati:
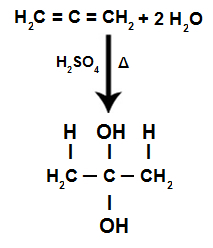
Equazione della reazione di idratazione dell'alcadiene accumulato
Abbiamo che nell'idratazione di un alcadiene accumulato, lo stesso atomo di carbonio riceve i due ossidrili, formando un alcol gemello, che è una struttura instabile.

Struttura del gemello formato alcol twin
Poiché l'alcool gemello è instabile, si ha la formazione di una molecola d'acqua con i componenti dei due ossidrili e la creazione di un legame pi greco tra carbonio e ossigeno.

Formazione di un chetone da un alcol gemello
Pertanto, la reazione di idratazione degli alcadieni accumulati porterà alla formazione di a chetone.
→ Alcadiene coniugato o alternativo
È un alcadiene che ha due doppi legami che coinvolgono contemporaneamente quattro atomi di carbonio, cioè c'è un singolo legame che separa i carboni coinvolti nei legami raddoppia.
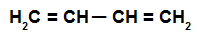
Formula di struttura di un alcadiene alternato
Negli alcadieni alternati si verifica la risonanza dei loro doppi legami. Pertanto, gli elettroni del legame pi greco cambiano posizione (frecce rosse), come nel diagramma seguente:
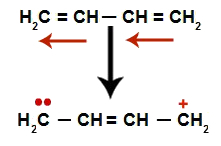
Schema raffigurante la risonanza in un alcadiene alternato
Abbiamo, in generale, l'apparenza di un doppio legame esattamente tra i carboni dove prima c'erano i due doppi e la creazione di due siti di legame, uno su ogni carbonio che non fa più il doppio legame (nell'esempio, i carboni 1 e 4). I carboni 1 e 4 della catena ricevono l'H+ e l'oh- dall'acqua.

Idratazione parziale in alcadiene alternato
Dopo la risonanza, il legame pi greco del nuovo doppio legame viene rotto e un H+ e un oh- vengono aggiunti alla molecola di alcadiene. L'OH viene aggiunto al carbonio più vicino al primo gruppo OH aggiunto perché subisce l'attrazione elettronica del gruppo, che è più elettronegativo.

Cessazione dell'idratazione in un alcadiene alternato
A causa della risonanza, diciamo che l'alcadiene alternato ha subito un'idratazione di 1,4, formando un dialcool.
→ Isolato in alcadiene
È un alcadiene che ha due doppi legami che coinvolgono almeno cinque atomi contemporaneamente. di carbonio, cioè ci sono almeno due singoli legami che separano i carboni coinvolti nei legami raddoppia.

Formula di struttura di un alcadiene isolato
Durante la reazione di idratazione di un alcadiene isolato, i legami pi sono rotti, l'H+ aggiunto ai carboni più idrogenati e agli OH- aggiunto ai carboni meno idrogenati.

Equazione della reazione di idratazione dell'alcadiene isolata
Pertanto, nell'aggiunta di un alcadiene isolato, si ha solo la formazione di un dialcool.
Di Me. Diogo Lopes Dias
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/quimica/reacoes-hidratacao-alcadienos.htm
