Acidi e basi sono due gruppi chimici correlati tra loro. Sono due sostanze di grande importanza e presenti nella vita di tutti i giorni.
Acidi e basi sono studiati dalla Chimica Inorganica, la branca che studia i composti che non sono formati dal carbonio.
Concetti di acidi e basi
Il concetto di Arrhenius
Uno dei primi concetti di acidi e basi sviluppati alla fine del XIX secolo da Svante Arrhenius, un chimico svedese.
Secondo Arrhenius, gli acidi sono sostanze che in soluzione acquosa soffrono ionizzazione, rilasciando come cationi solo H+.
HCl (acq) → H+ (aq) + Cl- (Qui)
Intanto le basi sono sostanze che soffrono dissociazione ionica, rilasciando gli ioni OH- (idrossile) come unico tipo di anione.
NaOH (aq) → Na+ (aq)+OH- (Qui)
Tuttavia, il concetto di Arrhenius per acidi e basi era limitato all'acqua.
Leggi anche su: Teoria di Arrhenius e Reazione di neutralizzazione.
Il concetto di Bronsted-Lowry
Il concetto di Bronsted-Lowry è più ampio di quello di Arrhenius ed è stato introdotto nel 1923.
Secondo questa nuova definizione, gli acidi sono sostanze capaci di donare un protone H
+ ad altre sostanze. E le basi sono sostanze in grado di accettare un protone H+ di altre sostanze.Questo è il l'acido è un donatore di protoni e la base è un recettore di protoni.
Caratterizza un acido forte come uno che si ionizza completamente in acqua, cioè rilascia ioni H+.
Tuttavia, la sostanza può essere anfiprotica, cioè capace di comportarsi come un acido o base Bronsted. Guarda l'esempio dell'acqua (H2O), una sostanza anfiprotica:
HNO3(ac) + H2oh(l) → NO3- (ac) + H3oh+(aq) = base di Bronsted, accettato il protone
NH3(ac) + H2oh(l) → NH4+(aq) + OH-(aq) = Acido Bronsted, donò il protone
Inoltre, le sostanze si comportano come coppie coniugate. Tutte le reazioni tra un acido e a base di Bronsted comportano il trasferimento di un protone e hanno due coppie acido-base coniugate. Vedi l'esempio:
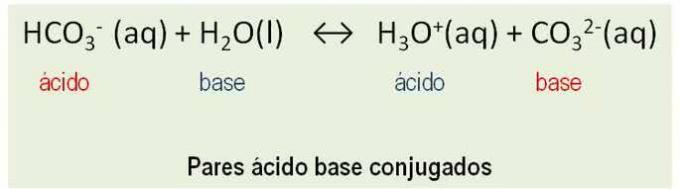
HCO3- e CO32-; H2O e H3oh+ sono coppie acido-base coniugate.
Impara di più riguardo:
- Funzioni inorganiche
- Indicatori acido-base
- Titolazione
nomenclatura degli acidi
Per definire la nomenclatura, gli acidi sono divisi in due gruppi:
- Idracidi: acidi senza ossigeno;
- Ossiacidi: acidi con ossigeno.
Idracidi
La nomenclatura si presenta come segue:
acido + nome elemento + idrico
Esempi:
HCl = acido cloridrico
HI = acido iodidrico
HF = acido fluoridrico
ossiacidi
La nomenclatura degli ossiacidi segue le seguenti regole:
voi acidi standard di ogni famiglia (famiglie 14, 15, 16 e 17 della Tavola Periodica) seguono la regola generale:
acido + nome elemento + ic
Esempi:
HClO3 = acido clorico
H2SOLO4 = acido solforico
H2CO3: acido carbonico
Per gli altri acidi che si formano con lo stesso elemento centrale, li chiamiamo in base alla quantità di ossigeno, seguendo la seguente regola:
| Quantità di ossigeno, in relazione all'acido standard | Nomenclatura |
|---|---|
| + 1 ossigeno | Acido + per + nome elemento + ico |
| - 1 ossigeno | Acido + nome elemento + osso |
| - 2 ossigeni | Acido + ipo + nome elemento + osso |
Esempi:
HClO4 (4 atomi di ossigeno, uno in più dell'acido standard): acido perclorico;
HClO2 (2 atomi di ossigeno, uno in meno dell'acido standard): acido cloroso;
HClO (1 atomo di ossigeno, due meno dell'acido standard): acido ipocloroso.
Potrebbero interessarti anche: acido solforico
Nomenclatura di base
Per la nomenclatura di base si segue la regola generale:
Idrossido + nome catione
Esempio:
NaOH = Idrossido di sodio
Tuttavia, quando lo stesso elemento forma cationi con cariche diverse, il numero della carica dello ione viene aggiunto alla fine del nome, in numeri romani.
Oppure puoi aggiungere il suffisso -oso, allo ione meno carico, e il suffisso -ico, allo ione più carico.
Esempio:
Ferro
Fede2+ = Fe(OH)2 = Idrossido di ferro II o Idrossido di ferro;
Fede3+ = Fe(OH)3 = Idrossido di ferro III o idrossido ferrico.
Assicurati di controllare le domande dell'esame di ammissione sull'argomento, con risoluzione commentata, in: Esercizi sulle funzioni inorganiche.



