La sublimazione è il passaggio dallo stato solido allo stato gassoso e viceversa, senza passare per lo stato liquido.
Affinché una sostanza possa subire il processo di sublimazione, deve essere sottoposta a determinati valori di temperatura e pressione.
Naftalina e CO2 solido (ghiaccio secco) sono esempi di sostanze che subiscono sublimazione in condizioni ambientali.

Diagramma delle fasi
Possiamo scoprire lo stato fisico di una sostanza conoscendo i valori di temperatura e pressione a cui è sottoposta.
Per questo, utilizziamo diagrammi costruiti per ogni sostanza, da valori trovati sperimentalmente.
Chiamato "Diagramma delle fasi", è diviso in tre regioni che rappresentano gli stati solido, liquido e gassoso. Le linee che delimitano queste regioni segnalano i punti in cui la sostanza cambia fase.
Il punto triplo nel diagramma indica la temperatura e la pressione alle quali la sostanza può coesistere nelle tre fasi. Al di sotto di questo punto c'è la curva di sublimazione.
I punti su questa curva determinano i valori di pressione e temperatura a cui avverrà la sublimazione.
Quando un solido è sottoposto a una pressione inferiore al punto triplo, se riscaldato passerà direttamente allo stato gassoso.
Il passaggio dallo stato solido diretto allo stato gassoso può avvenire anche diminuendo la pressione quando la sua temperatura è inferiore a quella del punto triplo.
Scopri di più su: Cambiamenti di stato fisico.
Diagramma di fase dell'anidride carbonica (CO)2 )
Il punto triplo della CO2 si verifica quando la pressione è di 5 atm. Questo fatto giustifica che è comune vedere il verificarsi della sublimazione nel ghiaccio secco, poiché la pressione ambiente è di 1 atmosfera.
Per questo motivo non si ottiene anidride carbonica liquida in condizioni ambientali. In queste condizioni si trova allo stato solido o allo stato di vapore.
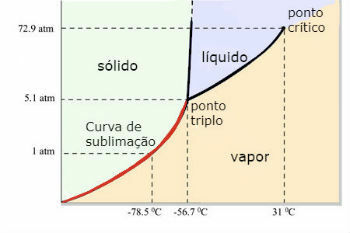
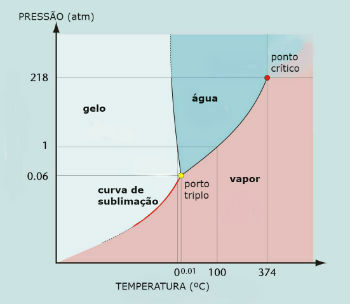
Diagramma di fase dell'acqua (H2o)
Il punto triplo dell'acqua si verifica quando la pressione è di soli 0,06 atm. Pertanto, in condizioni ambientali non è comune che l'acqua sublimi.
Per saperne di più leggi anche:
- Stati fisici dell'acqua
- Stati fisici della materia
- Liquefazione o condensazione
- Proprietà della materia
- solidificazione
- Fusione
- Vaporizzazione
- Bollente
- Evaporazione